

| A. | 2 Ag(s)+Cd2+( aq)═2 Ag+(aq)+Cd(s) | B. | Co2+( aq)+Cd(s)═Co(s)+Cd2+( aq) | ||
| C. | 2 Ag+(aq)+Cd(s)═2Ag(s)+Cd2+( aq) | D. | 2Ag+( aq)+Co( s)═2 Ag(s)+Co2+( aq) |
分析 原电池中负极上易失去电子,则负极金属材料的活动性较强,左边装置中,铬作负极,钴作正极,所以铬的活动性比钴强,右边装置中,钴作负极,银作正极,所以钴的活动性比银强,根据以上反应知,金属的活动性顺序为Cd>Co>Ag,金属的活动性越强,则金属的还原性越强.
解答 解:根据原电池的正负极知,金属的活动性顺序为:Cd>Co>Ag,金属的活动性越强,则金属的还原性越强,
A.反应2 Ag(s)+Cd2+(aq)═2 Ag+(aq)+Cd(s)中,Ag的还原性大于铬,与已知不符,故A错误;
B.反应Co2+(aq)+Cd(s)═Co(s)+Cd2+(aq)中,铬的还原性大于钴,与已知相符,故B正确;
C.反应2 Ag+(aq)+Cd(s)═2Ag(s)+Cd2+(aq)中,铬的还原性大于银,与已知相符,故C正确;
D.反应2Ag+(aq)+Co(s)═2 Ag(s)+Co2+(aq)中,钴的还原性大于银,与已知相符,故D正确;
故选A.
点评 本题以原电池原理为载体考查了金属还原性强弱、离子方程式书写,题目难度中等,注意失电子能力越强的金属其还原性越强,明确原电池工作原理为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
| 金属的用途 | 对应的金属物理性质 |
| 金可制成比纸还薄的金箔 | ③ |
| 用铁、铝等做炊具 | ② |
| 用铜制作印刷电路 | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.2 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 | |
| B. | 将0.001 mol•L-1的AgNO3溶液滴入0.001 mol•L-1的KCl和0.001 mol•L-1的K2CrO4溶液中,先产生Ag2CrO4沉淀 | |
| C. | c(Mg2+)为0.11 mol•L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上 | |
| D. | 在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M(X)>M(Y) | B. | M(X)<M(Y) | C. | M(X)=M(Y) | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
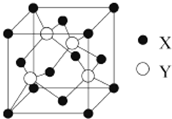 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; .
. .
.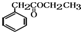 )的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任选).合成路线流程图示例如下: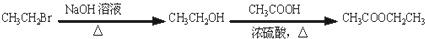
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池工作时两极质量均增加 | |
| B. | Fe上镀Ag时,Ag接电源的正极 | |
| C. | 精炼铜时,阳极有0.2 molCu氧化阴极就有0.1 molCu2+被还原 | |
| D. | 用惰性电极电解饱和NaCl溶液和KNO3溶液,阴极都得到H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com