
| A. | 0.1mol/L的Na 2A溶液中:c(A 2-)+c(HA -)+c(H 2A)=0.1mol/L | |
| B. | 常温下,将pH=3的H 2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 | |
| C. | 常温下,将pH=3的H 2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 | |
| D. | 常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na +)-c(HA -)-c(A 2-)=10 -5-10 -9 |
分析 A.溶液中存在物料守恒;
B.已知H 2A为弱酸,常温下,将pH=3的H 2A溶液稀释到原来的100倍,促进电离平衡正向进行;
C.常温下,将pH=3的H 2A溶液与pH=11的NaOH溶液等体积混合,平衡状态下氢离子和氢氧根离子反应后,又电离出氢离子;
D.结合溶液中的电荷守恒计算分析判断.
解答 解:A.0.1mol/L的Na 2A溶液中存在物料守恒,A2-离子分步水解,A2-离子的存在形式总和为0.1mol/L:c(A 2-)+c(HA -)+c(H 2A)=0.1mol/L,故A正确;
B.已知H 2A为弱酸,溶液中存在电离平衡,常温下,将pH=3的H 2A溶液稀释到原来的100倍,促进电离平衡正向进行,又电离出氢离子,则稀释后溶液的pH<5,故B正确;
C.常温下,将pH=3的H 2A溶液与pH=11的NaOH溶液等体积混合,溶液反应酸又电离出氢离子,混合液呈酸性,故C正确;
D.常温下,若1mol/L的NaHA溶液的pH=9,溶液中c(H+)=10-9mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-9}}$=10-5mol/L,溶液中电荷守恒c(Na +)+c(H+)=c(HA -)-2c(A 2-)+c(OH-),c(Na +)-c(HA -)-2c(A 2-)=10 -5-10 -9,故D错误;
故选D.
点评 本题考查了电解质溶液中电荷守恒、电离平衡、物料守恒、酸碱反应后溶液耐碱性、离子积常数的判断等知识点,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
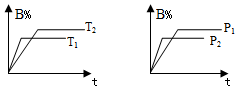 已知某可逆反应:aA(g)+bB (g)?cC(g) 在密闭容器中进行反应,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合物气体中物质的量百分含量(B%)的关系曲线:由曲线分析出:(填写<、>或=)
已知某可逆反应:aA(g)+bB (g)?cC(g) 在密闭容器中进行反应,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合物气体中物质的量百分含量(B%)的关系曲线:由曲线分析出:(填写<、>或=)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
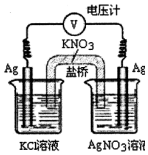 实验室利用如图所示装置,通过测电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
实验室利用如图所示装置,通过测电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 该装置工作时电能转化为化学能 | |
| B. | 左池中的电极增重比右池中电极更大 | |
| C. | 盐桥中的K+向左池方向移动 | |
| D. | 总反应为Ag+(aq)+C1-(aq)=AgCl(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 离子反应与复分解反应属于包含关系 | |
| B. | 化合物与电解质属于包含关系 | |
| C. | 金属氧化物与碱性氧化物属于交叉关系 | |
| D. | 氧化还原反应与化合反应属于并列关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中的氧化剂只有Cu2O | |
| B. | Cu2O在反应中既是氧化剂又是还原剂 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | 氧化产物与还原产物的物质的量之比为1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=l的溶液中:K+、Na+、NO3-、CH3COO- | |
| B. | Na2S溶液中:K+、Na+、NO3-、Ag+ | |
| C. | KC1溶液中:Na+、Fe3+、SO42-、SCN- | |
| D. | c(OH-)=1×10-13 mol•L-1的溶液中:K+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 铝具有强还原性 | 可用铝与浓硫酸反应制备氢气 |
| B | Fe(OH)2稳定 | 用FeCl2溶液和NaOH溶液反应可制取纯净的Fe(OH)2 |
| C | Na2O2与CO2反应生成氧气 | Na2O2可作供氧剂 |
| D | 二氧化硅不与任何酸反应 | 可用二氧化硅制造耐酸容器 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com