
(9分)氮元素可形成多种离子,如N3—、N3—、NH2—、NH4+、N2H5+、N2H62+等。
(1)与N相邻的两种元素C、O,三者第一电离能由大到小为_______
(2)N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1,说明N2中的 键比 键稳定(填“σ”或“π”)。
(3)液态氨可电离出NH2-。NH2-的电子式为 。
(4)已知NH4H为离子化合物,写出其与重水D2O反应的生成物(加热) ;Na3N也为离子化合物,则Na3N与水反应的化学方程式为 ,反应类型为 。
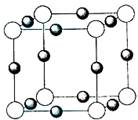
(5)X+中所有电子正好充满K、L、M三个电子层,它与N3—形成的晶体结构如图所示。与同一个N3—相连的X+ 有 个。X原子的基态电子排布式为_____________
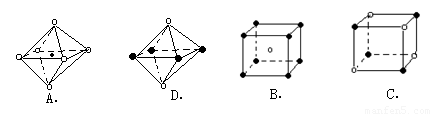
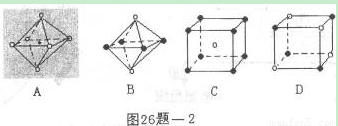
(6)最近科学家研制出某元素Z与N元素形成的晶体ZN,已知ZN晶体具有与NaCl相似的晶体结构。下图是从ZN晶体结构图中分割出来的部分结构图,试判断符合ZN晶体结构图的是_______
|
(1)N>O>C
(2)π
σ (3)
(4)HDO、HD、和NH3 Na3N+3H2O=3NaOH+NH3↑ 复分解反应(或水解反应)
(5) 6 1s22s22p63s23p63d104s1 (6) AD
【解析】
试题分析:(1)同周期随着原子序数的增加,第一电离能逐渐增加,但是IIA、IIIA族反常,VA、VIA族反常。所以C、N、O的第一电离能N>O>C。(2)N2中存在一个σ键和2个π键,又知N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1,可求得π键键能为347.5 kJ·mol-1,所以π键比σ键稳定。(3)NH2-为NH3失去一个氢离子得到的离子,其电子式为 。(4)NH4H与D2O反应时,NH4H电离出来的NH4+离子与D2O电离出来的OD-结合生成NH3和HDO,NH4H电离出来的H-与D2O电离出来的D+反应生成HD,因此产物为HDO、HD、和NH3。Na3N与水反应的化学方程式为Na3N+3H2O=3NaOH+NH3↑。(5)X+中所有电子正好充满K、L、M三个电子层,则X的电子排布式为1s22s22p63s23p63d104s1。根据晶胞结构可以看出与同一个N3-相连的X+有6个。(6)NaCl晶胞中一个Na+周围有6个Cl-,一个Cl-周围有6个Na+,ZN晶体具有与NaCl相似的晶体结构,所以符合的结构为AD。
。(4)NH4H与D2O反应时,NH4H电离出来的NH4+离子与D2O电离出来的OD-结合生成NH3和HDO,NH4H电离出来的H-与D2O电离出来的D+反应生成HD,因此产物为HDO、HD、和NH3。Na3N与水反应的化学方程式为Na3N+3H2O=3NaOH+NH3↑。(5)X+中所有电子正好充满K、L、M三个电子层,则X的电子排布式为1s22s22p63s23p63d104s1。根据晶胞结构可以看出与同一个N3-相连的X+有6个。(6)NaCl晶胞中一个Na+周围有6个Cl-,一个Cl-周围有6个Na+,ZN晶体具有与NaCl相似的晶体结构,所以符合的结构为AD。
考点:物质结构
点评:本题是物质结构综合性习题,(4)与(6)两个小题难度较大。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源:2011-2012学年重庆市高三9月月考理科综合试题(化学部分) 题型:填空题
(14分)氮是地球上极为丰富的元素,氮元素可形成多种离子,如:N3—、N3—、NH2—、NH4+、N2H5+、N2H62+等。
(1)请画出氮的原子结构示意图___________。
(2)氮的常见氢化物的结构式为________,其空间构型为_______,它极易溶于水的主要原因是_________________,溶于水后显碱性的原因是_______________(用离子方程式说明)
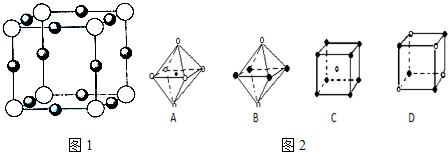
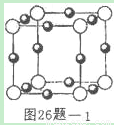
(3)X+中所有电子正好充满K、L两个电子层,它与N3—形成的晶体结构如图26题 l所示。与同一个N3—相连的X+有________个,X的元素符号是________。
(4)最近科学家研制出某元素Z与N元素形成的晶体ZN,已知ZN晶体具有与NaCI相似的晶体结构。图26题-2是从ZN晶体结构图中分割出来的部分结构图,试判断符合ZN晶体结构图的是_______________。
查看答案和解析>>
科目:高中化学 来源:0113 期中题 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:
(08浙江舟山中学月考)氮元素可形成多种离子,如N3―、N3―、NH2―、NH4+、N2H5+、N2H62+等,其中N2H62+是由中性分子结合质子形成的,有类似于NH4+的性质。回答下列问题:
(1)N3―离子半径比Na+离子半径 (填“大”或“小”)
(2)写出Na3N与水反应的化学方程式
(3)NH4+离子中N―H键的键角为 ,写出离子化合物NH5的电子式
(4)写出N2H62+离子与过量强碱溶液反应的离子方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com