
(14 分) 在我国冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为![]() ,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol
,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol ![]() 含有54 mol电子。
含有54 mol电子。
(1)该融雪剂的化学式是____________,X与氢元素形成的化合物的电子式___________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________________;D与E能形成一种非极性分子,该分子的结构式为___________________;D所在族元素的氢化物中,沸点最低的是___________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子![]() 中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是______________。
中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是______________。
(4)元素R与Y同主族,其氢化物能用于腐蚀玻璃,![]() 与
与![]() 溶液反应的产物之一是
溶液反应的产物之一是![]() ,该反应的离子方程式是____________________________。
,该反应的离子方程式是____________________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
1999年11月20日,我国酒泉卫星发射中心成功发射了“神舟”号载人试验飞船。飞船绕地球14圈后,地面控制中心发出返回指令,飞船启动制动发动机、调整姿态后,在内蒙古中部平安降落。
(1)假定飞船速度为7.72×103m/s,沿离地面高度为300km的圆轨道运行,轨道半径为 ;其运行周期为 分;在该高度的重力加速度为 (已知地球半径为6.4×103km,地球质量为6.0×1024kg,万有引力恒量G=6.67×10-11N·m2/kg2)。
(2)飞船脱离原来轨道返回大气层的过程中,其重力势能将 ,动能将 ,机械能将 。(均填增大或减小或不变)
(3)将生物随飞船带入太空,可进行多项科学研究。如植物种子经太空返回地面后种植,往往能得到新的变异特性。这种变异的来源主要是植物种子经太空中的 辐射后,其 发生变异。现一般把这种育种方式称为 。试举出这种育种方式的一个优点: 。
(4)在宇宙飞船中为了使宇航员得到一个稳定的、良好的生存环境,一般在飞船内安装了盛有Na2O2颗粒的装置,它的用途是再生氧气。如用KO2(超氧化钾)代替Na2O2能达到同样的目的,反应产物也很相似。
①写出超氧化钾与CO2反应的化学方程式 。
②计算用Na2O2和KO2分别与CO2反应,产生等量的氧气,所需Na2O2和KO2的质量比为1︰ (精确到小数点后一位)。
(5)建国后,特别是改革开放以来,我国航天事业迅速发展,该飞船的成功发射,显示了我国 的增强。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省枣强县中学高一下学期期末考试化学试卷(带解析) 题型:填空题
(14分)阅读讨论并完成以下各项内容:
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02 mg/L。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的SO2和氮的氧化物。它们的主要来源是煤和石油的燃烧,全世界每年排放1.5亿吨的SO2。
①SO2可在空气中受光照等因素作用而被氧化,最终与雨水形成硫酸型酸雨。试写出这两个化学反应的方程式
________________________________________________________________________;
________________________________________________________________________。
②汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成 ________和NO。
③酸雨可导致的危害有________(填序号)。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
④为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫化物进行________,对废气中的氮的氧化物用________吸收。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量(已知碘能氧化H2SO3,生成H2SO4)。
①若原料气从左向右流时,上述装置连接的顺序是:原料气→________(用字母和箭头表示)。
②装置②中发生反应的离子方程式为:
________________________________________________________________________;
当装置②中出现________现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是________。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
查看答案和解析>>
科目:高中化学 来源:2012-2013年湖北省仙桃市毛嘴高中高一上学期学业水平监测试化学卷(带解析) 题型:填空题
(14分)2010年在我国北方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图为  ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=_____,该融雪剂的化学式为_______。
(2)Z、W元素名称分别为_______、_______。
(3)下列说法正确的是________。
A.XY2和WZ2都为离子化合物
B.XY2中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。
A.XY2的电子式:X2+[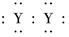 ]2-
]2-
B.WZ2的结构式:Z===W===Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-===2Y-+Z↓
D.用电子式表示XY2的形成过程为:
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是
。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年甘肃白银市平川中恒学校高一下学期期末考试化学试卷(带解析) 题型:填空题
(14分)阅读并完成以下各项内容:
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02 mg/L。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的SO2和氮的氧化物。它们的主要来源是煤和石油的燃烧,全世界每年排放1.5亿吨的SO2。
①SO2可在空气中受光照等因素作用而被氧化,最终与雨水形成硫酸型酸雨。试写出这两个化学反应的方程式:________________ , 。
②汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成 ________和NO。
③酸雨可导致的危害有________(填序号)。
A.腐蚀建筑物 B.导致树木枯萎 C.造成洪涝灾害 D.恶化人类环境
④为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫化物进行________,对废气中的氮的氧化物用________吸收。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量(已知碘能氧化H2SO3,生成H2SO4)。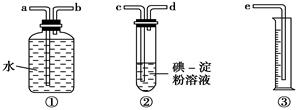
①若原料气从左向右流时,上述装置连接的顺序是:原料气→________ (用字母和箭头表示)。
②装置②中发生反应的离子方程式为: ;
当装置②中出现________现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是________。
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
查看答案和解析>>
科目:高中化学 来源:2014届河北省高一下学期期末考试化学试卷(解析版) 题型:填空题
(14分)阅读讨论并完成以下各项内容:
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02 mg/L。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的SO2和氮的氧化物。它们的主要来源是煤和石油的燃烧,全世界每年排放1.5亿吨的SO2。
①SO2可在空气中受光照等因素作用而被氧化,最终与雨水形成硫酸型酸雨。试写出这两个化学反应的方程式
________________________________________________________________________;
________________________________________________________________________。
②汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成 ________和NO。
③酸雨可导致的危害有________(填序号)。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
④为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫化物进行________,对废气中的氮的氧化物用________吸收。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量(已知碘能氧化H2SO3,生成H2SO4)。

①若原料气从左向右流时,上述装置连接的顺序是:原料气→________(用字母和箭头表示)。
②装置②中发生反应的离子方程式为:
________________________________________________________________________;
当装置②中出现________现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是________。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com