
| A、盐酸 | B、稀硝酸 |
| C、氨水 | D、氢氧化钠溶液 |
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:

| 一系列 |
| 操作 |
| ①酸性高锰酸钾 |
| ②(NH4)2Fe(SO4)2 |
| 标准溶液滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 将水蒸气通过灼热的铁粉,粉末变红褐色 | 铁与水在高温下发生反应 |
| B | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中不一定含有Fe2+ |
| C | 将某气体通入酸性高锰酸钾溶液中,溶液紫色褪去 | 该气体有还原性 |
| D | 用PH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若生成1 molP(g),则放出的热量等于a kJ |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(Y)=0.100mol/L,则c(P)=0.0203 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤的方法除去食盐水中的泥沙 |
| B、用蒸馏的方法将自来水制成蒸馏水 |
| C、用酒精萃取碘水中的碘 |
| D、用加热的方法除去苏打中的小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
| 3%溴水 |
| 55℃ |
| 过量CaCO3 |
| 70℃ |
| 趁热过滤 |
| 乙醇 |
| 过滤 |
| 洗涤 |
| 干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
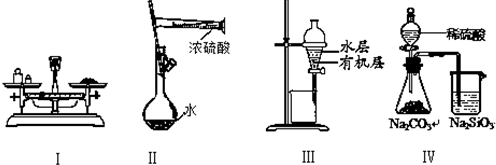
| A、实验Ⅰ:用托盘天平称量一定质量的氯化钠固体 |
| B、实验Ⅱ:配制一定物质的量浓度的硫酸 |
| C、实验Ⅲ:用苯萃取溴水中的溴后进行分液 |
| D、实验Ⅳ:比较硫酸、碳酸和硅酸酸性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高于河水 |
| B、蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖 |
| C、不可用铝制餐具长时间存放酸性、碱性食物 |
| D、凡含有食品添加剂的食物对人体健康均有害,不宜食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应物总能量小于成物总能量 |
| B、断键和成键过程中都释放能量 |
| C、断键过程中吸收能量,成键过程中释放能量 |
| D、断键过程中释放能量,成键过程中吸收能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com