
| A、碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B、氯气溶于水:Cl2+H2O?2H++Cl-+ClO- |
| C、亚硫酸氢钠溶液中滴加硫酸氢钠溶液:H++HSO3-=SO2↑+H2O |
| D、氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、第二周期氢化物易燃性:CH4<NH3<H2O( ) |
| B、第三周期氢化物稳定性:SiH4>PH3>H2S>HCl |
| C、化合物毒性:若PH3>NH3,则H2S>H2O |
| D、氢化物的还原性:HF>H2O>NH3>CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 |
| 甲同学:取少量(0.5~2mL)小烧杯中的溶液于洁净试管中,滴加1~2滴20%KSCN溶液 | ①若溶液显血红色,则假设 ②若溶液不发生颜色变化,则假设 |
乙同学: | ③若粉末 ④若粉末 ⑤若粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:
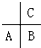 短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )
短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )| A、若均为非金属元素,其气态氢化物稳定性:A<B<C |
| B、若均为金属元素,其最高价氧化物的水化物的碱性:A<B<C |
| C、原子半径:A>C>B |
| D、最高正价:A>B>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| A、中子数为1 |
| B、质子数为2 |
| C、质量数为3 |
D、原子结构示意图是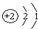 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤⑥ |
| B、②⑤④①③⑥ |
| C、①②④⑤③⑥ |
| D、④②③①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
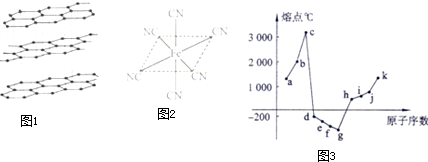
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com