
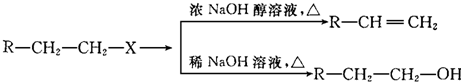

| 醇 |
| △ |
| H2O |
| △ |
| 醇 |
| △ |
| H2O |
| △ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计实验探究构成原电池的条件,装置如下:
某同学设计实验探究构成原电池的条件,装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:
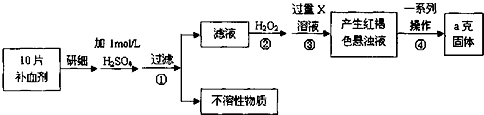
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、21.2 g |
| B、21.6 g |
| C、22.0 g |
| D、22.3 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过滤时,漏斗的下端应紧贴烧杯内壁 |
| B、给试管中的液体加热时,可以用手直接拿试管 |
| C、给试管中的固体加热时,试管口应略向上倾斜 |
| D、蒸馏液体时,冷水应从冷凝管的上端进入,下端出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粗盐提纯操作的顺序是:溶解、过滤、蒸发、洗涤 |
| B、实验室制取氧气完毕后,应先取出集气瓶,再取出导管,最后停止加热 |
| C、不慎将浓硫酸洒在桌上,应先用烧碱溶液中和,再用湿布抹净 |
| D、用试管夹夹持试管时,把试管夹从试管底部往上套,夹在试管中上部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
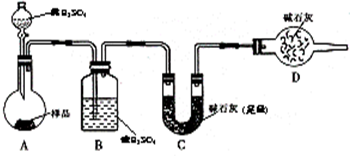
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com