
在C(s)+CO2(g) 2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强②增加碳的量 ③通入CO2 ④恒容下充入He ⑤恒压下充入He ⑥加热,其中能够使反应速率增大的措施是( )
2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强②增加碳的量 ③通入CO2 ④恒容下充入He ⑤恒压下充入He ⑥加热,其中能够使反应速率增大的措施是( )
A.①④ B.②③⑤ C.①③⑥ D.①②④
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学卷(解析版) 题型:选择题
标准状况下有①6.72LCH4;②3.01X1023个HCl;③13.6gH2S;④0.2molNH3.下列对四种气体的关系从小到大表示不正确的是
A.体积:④<①<②<③ B.密度:①<④<③<②
C.质量:④<①<③<② D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上10月月考化学卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2(g)  2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上月考一化学试卷(解析版) 题型:选择题
将1体积A(g)和3体积B(g)混合,在5000C和催化剂存在下发生如下反应:2A(g)+B(g) 2C (g)并达到平衡状态,在同温同压下测得此反应在平衡前后的气体密度之比为9/10,此时A的转化率( )
2C (g)并达到平衡状态,在同温同压下测得此反应在平衡前后的气体密度之比为9/10,此时A的转化率( )
A.90% B.80% C.45% D.10%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上月考一化学试卷(解析版) 题型:选择题
已知:2H2(g) + O2(g) = 2H2O(l) △H = -571.6 kJ·mol-1 ,CH4(g) + 2O2(g)= CO2(g) + 2H2O(l) △H = -890 kJ·mol-1 ,现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是
A.1:1 B.1:3 C.1:4 D.2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上月考一化学试卷(解析版) 题型:填空题
2016年9月3日,二十国集团领导人杭州峰会之前,中国政府率先签署了《巴黎协定》并向联合国交存批准文书,体现中国为应对全球气候变化做出了重要贡献。为减少CO2对环境造成影响,有科学家提出设想,先把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇,流程如下:
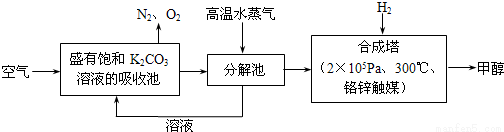
(1)写出分解池中反应的化学方程式___________________。
(2)在合成塔中,当有8.8gCO2与足量H2完全反应,可放出9.84×l03kJ的能量,写出合成塔中反应的热化学方程式______________________。
(3)在体积为l L的密闭容器中,充入1molCO2和3molH2在300℃下发生反应,有关物质的浓度随时间变化如下图所示。
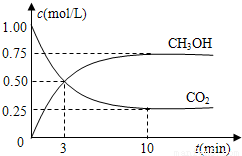
①从反应开始到平衡,H2的平均反应速率v(H2)=_______ _____。
②其他条件不变,只将温度提高到500℃,再次平衡时n(CH3OH)/n(CO2)比值___________(填“增大”、“减小”或“不变”)。
③从平衡移动原理分析,低温有利于提高原料气的转化率,而实际生产中采用300℃的温度,原因是_______________。
(4)目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H>0。
CH3OCH3(g)+3H2O(g) △H>0。
判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是_________。
a.容器中密度不变
b.单位时间内消耗2molCO2,同时消耗1mol二甲醚
c.v(CO2):v(H2)=1:3
d.容器内压强保持不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上月考一化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可以制取氯化硫酰( SO2Cl2):SO2(g)+Cl2(g) SO2C12(l) △H<0,在恒压密闭容器中,加入1mol SO2和1mol Cl2,反应达到平衡后,当其他条件不变时,下列说法正确的是( )
SO2C12(l) △H<0,在恒压密闭容器中,加入1mol SO2和1mol Cl2,反应达到平衡后,当其他条件不变时,下列说法正确的是( )
A.再加入1mol SO2和1mol Cl2,重新达到平衡后,Cl2浓度和原平衡时相等
B.升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.通入Ar气,使容器压强增大,可同时提高SO2和Cl2的转化率
D.分离出部分SO2Cl2,正反应速率增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上9月月考化学试卷(解析版) 题型:填空题
碳及其化合物与人类的生活、生产紧密联系。
(1)已知1g甲烷完全燃烧生成稳定的氧化物时放出Q kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(2)已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+130 kJ·mol-1,
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1。断开1 mol H—H键、O===O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键需要吸收的热量为
A.332 kJ B.118 kJ
C.462 kJ D.360 kJ

(3)以CO2和H2O为原料制备HCOOH和O2的原电池原理如图.电极a、b表面发生的电极反应式分别为:
a: ,b: .

(4)图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2气体。则阳极产生ClO2的电极反应式为_______________________,用平衡移动原理解释阴极区pH增大的原因:_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考一化学试卷(解析版) 题型:选择题
在0.5molNa2SO4中含有Na+的数目是
A.3.01x1023 B.6.02x1023 C.0.5 D.1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com