
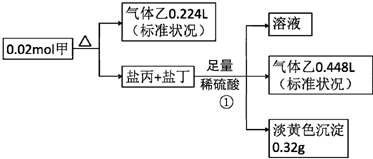
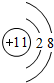 ,甲的化学式Na2S2O4
,甲的化学式Na2S2O4分析 甲的焰色为黄色,含有Na元素,盐丙和丁的组成元素和甲相同,加入足量硫酸反应生成的乙能使品红溶液褪色,则乙为SO2,生成的淡黄色沉淀为S,丙、丁中其中一种为Na2S2O3,发生反应:Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O,反应①生成的二氧化硫为$\frac{0.448L}{22.4L/mol}$=0.02mol,硫为0.32g即0.01mol,而Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O中生成的S、SO2均为0.01mol,故丙、丁中其中一种为Na2SO3,发生反应:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,该反应生成SO2为0.02mol-0.01mol=0.01mol,结合方程式可知,Na2S2O3为0.01mol,Na2SO3为0.01mol,甲分解得到二氧化硫为$\frac{0.32g}{22.4L/mol}$=0.01mol,根据原子守恒可知,0.02mol甲中含有:Na原子为0.01mol×2+0.01mol×2=0.04mol,S原子为0.01mol+0.01mol×2+0.01mol=0.04mol,O原子为(0.01mol+0.01mol)×3+0.01mol×2=0.08mol,则1mol甲含有2molNa原子、2molS原子、4molO原子,故甲的化学式为Na2S2O4,据此解答.
解答 解:甲的焰色为黄色,含有Na元素,盐丙和丁的组成元素和甲相同,加入足量硫酸反应生成的乙能使品红溶液褪色,则乙为SO2,生成的淡黄色沉淀为S,丙、丁中其中一种为Na2S2O3,发生反应:Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O,反应①生成的二氧化硫为$\frac{0.448L}{22.4L/mol}$=0.02mol,硫为0.32g即0.01mol,而Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O中生成的S、SO2均为0.01mol,故丙、丁中其中一种为Na2SO3,发生反应:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,该反应生成SO2为0.02mol-0.01mol=0.01mol,结合方程式可知,Na2S2O3为0.01mol,Na2SO3为0.01mol,甲分解得到二氧化硫为$\frac{0.32g}{22.4L/mol}$=0.01mol,根据原子守恒可知,0.02mol甲中含有:Na原子为0.01mol×2+0.01mol×2=0.04mol,S原子为0.01mol+0.01mol×2+0.01mol=0.04mol,O原子为(0.01mol+0.01mol)×3+0.01mol×2=0.08mol,则1mol甲含有2molNa原子、2molS原子、4molO原子,故甲的化学式为Na2S2O4,
(1)甲为Na2S2O4,甲中所含阳离子的结构示意图为: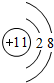 ,
,
故答案为: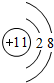 ;Na2S2O4;
;Na2S2O4;
(2)①中产生黄色沉淀的反应的离子反应方程式:S2O32-+2H+=S↓+SO2↑+H2O,
故答案为:S2O32-+2H+=S↓+SO2↑+H2O;
(3)乙为二氧化硫,能与品红结合生成不稳定的无色化合物,使品红溶液褪色,
故答案为:能与品红结合生成不稳定的无色化合物;
(4)Na2S2O4的溶液还可用作分析化学中的吸氧剂,假设其溶液与少量氧气反应产生等物质的量的两种酸式盐,硫元素化合价升高,反应生成NaHSO3、NaHSO4,该反应的化学反应方程式:Na2S2O4+O2+H2O=NaHSO3+NaHSO4,
故答案为:Na2S2O4+O2+H2O=NaHSO3+NaHSO4;
(5)甲具有还原性,氯气具有氧化性,硝酸银溶液显酸性,具有氧化性,二者可能与甲反应,
故选:BC.
点评 本题考查无机物推断,属于计算型推断,关键是根据气体乙的性质及淡黄色沉淀判断丙、丁其中一种为Na2S2O3,需要学生具备扎实的基础,难度较大.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | 水既不显酸性又不显碱性 | |
| B. | 水既是氧化剂又是还原剂 | |
| C. | 钠既容易被氧化又容易被还原 | |
| D. | 该反应既是置换反应又是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸及其钠盐可用作乳胶、牙膏、果酱及其它食品的防腐剂,也可用作染色和印色的媒染剂.某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸,制备原理和实验主要装置甲如下:
苯甲酸及其钠盐可用作乳胶、牙膏、果酱及其它食品的防腐剂,也可用作染色和印色的媒染剂.某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸,制备原理和实验主要装置甲如下:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应的速率越大,化学反应的限度越大 | |
| B. | 质量数不同的原子互称同位素 | |
| C. | 糖类、油脂、蛋白质都能发生水解 | |
| D. | 油脂有油和脂肪之分,但都属于酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向该容器中增加CO的量可加大反应速率 | |
| B. | 增大H2的用量,有可能使CO转化率达到100% | |
| C. | 使用合适的催化剂、升高温度均可加大反应速率 | |
| D. | 在一定条件下,当CO的浓度不再改变时,反应达到最大限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L | B. | 0.2 mol/L | C. | 0.4 mol/L | D. | 0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL量筒的0刻度在最下方 | |
| B. | 天平上游码标尺最左方的刻度为0 | |
| C. | 一般温度计的0刻度在中间位置 | |
| D. | 容量瓶的刻度无数字,只是瓶颈上的一个水平环 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com