
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| C. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| D. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
分析 Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明溶液中一定含有K+;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成,证明含有NO3-、Fe2+,一定不含有SiO32-、CO32-;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,即为硫酸钡,证明含有SO42-,再滴加KSCN溶液,上层清液变红,即出现了三价铁离子,是Ⅱ过程中亚铁离子被硝酸氧化的结果;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色,证明没有碘单质,一定没有I-,Cl-是否存在无法确定,据此进行解答.
解答 解:某溶液中含K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-中的若干种,
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明溶液中一定含有K+;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成,证明含有NO3-、Fe2+,一定不含有SiO32-、CO32-;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,即为硫酸钡,证明含有SO42-,再滴加KSCN溶液,上层清液变红,即出现了三价铁离子,是Ⅱ过程中亚铁离子被硝酸氧化的结果;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色,证明没有碘单质出现,一定没有I-,Cl-是否存在无法确定,
A.原溶液中一定含有NO3-、Fe2+,故A错误;
B.原溶液中一定不含I-,故B错误;
C.根据分析可知,步骤Ⅱ中无色气体是NO气体,无CO2气体产生,故C正确;
D.原溶液中含有硫酸根离子,干扰了氯离子的检验,故D错误;
故选C.
点评 本题考查常见离子的检验、鉴别以及方程式的有关计算,题目难度中等,解答本题的关键是根据发生的有关化学反应确定存在的离子,注意掌握常见离子的性质及检验方法.


科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| B. | 铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 | |
| C. | 氢氧燃料电池的能量转换形式之一为化学能转化为电能 | |
| D. | 催化剂通过降低化学反应的焓变加快化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的化学方程式及室温下的平衡常数如下:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的化学方程式及室温下的平衡常数如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ),M的一种合成路线如图(部分反应试剂和条件省略).
),M的一种合成路线如图(部分反应试剂和条件省略).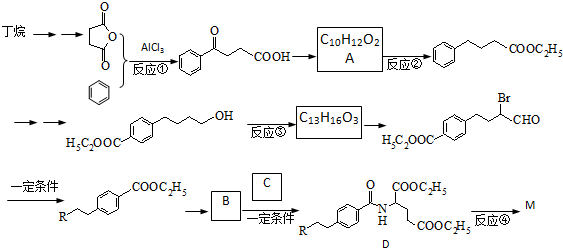
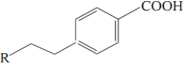 ,C
,C ;
;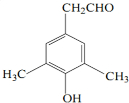 或
或
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 W、X、Y、Z分别为H、C、N、O元素
W、X、Y、Z分别为H、C、N、O元素查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钾和氧化汞都属于氧化物 | B. | 氧气和臭氧都属于单质 | ||
| C. | 碳酸钙和甲烷都属于有机物 | D. | 火碱和纯碱都属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2Cl2+Br2$\stackrel{光照}{→}$CHBrCl2+HBr | |
| B. | CH3OH+HCl→CH3Cl+H2O | |
| C. | CH3-CH2-Br+H2O$\stackrel{NaOH}{→}$CH3-CH2-OH+HBr | |
| D. | 2Na+2H2O═2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol•L-1Na3PO4溶液 | B. | 75 mL 2 mol•L-1NaNO3溶液 | ||
| C. | 75 mL 3 mol•L-1Na2SO4溶液 | D. | 150 mL 2mol•L-1 CH3COONa溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{1000ρw}{M}$ | B. | m=V•ρ•$\frac{w}{100}$ | C. | w=$\frac{cM}{1000ρ}$ | D. | c=$\frac{1000m}{MV}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com