
| A. | 9 g H2O所含有的电子数为5NA | |
| B. | 1 mol MgCl2中含有离子数为NA | |
| C. | 1 L 0.1 mol•L-1 Na2SO4溶液中有0.1NA 个Na+ | |
| D. | 1 mol C10H20分子中原子总数为13NA |
分析 A、求出水的物质的量,然后根据水中含10个电子来分析;
B、氯化镁由1个镁离子和2个氯离子构成;
C、求出硫酸钠的物质的量,然后根据1mol硫酸钠中含2mol钠离子来分析;
D、C10H20中含10个碳原子和20个H原子.
解答 解:A、9g水的物质的量为0.5mol,而水中含10个电子,故0.5mol水中含5NA个电子,故A正确;
B、氯化镁由1个镁离子和2个氯离子构成,故1mol氯化镁中含3NA个离子,故B错误;
C、溶液中硫酸钠的物质的量n=CV=0.1mol/L×1L=0.1mol,而1mol硫酸钠中含2mol钠离子,故0.1mol硫酸钠中含0.2NA个钠离子,故C错误;
D、C10H20中含10个碳原子和20个H原子,故1mol此烃中含30NA个原子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
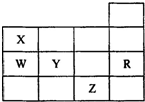 表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )
表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )| A. | 常温常压下,五种元素的单质中有两种是气态 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | W的氢化物比X的氢化物沸点高 | |
| D. | Y与W元素的最高价氧化物对应的水化物的酸性比较,前者弱于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、NO3-、H+、Ag+ | B. | K+、Fe3+、Cl-、SO42- | ||
| C. | K+、Ba2+、Cl-、CO32- | D. | Na+、AlO2-、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量燃烧化石燃料及汽车尾气是造成雾霾天气的重要因素 | |
| B. | 冬天严禁在窗门紧闭的室内用煤饼炉取暖,因为生成的CO、SO2等容易引起中毒 | |
| C. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| D. | 氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全地带 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可用于保存海鲜产品 | |
| B. | 硅胶吸附能力强,常用作催化剂载体和食品干燥剂 | |
| C. | 糖类、油脂、蛋白质在一定条件下都可以发生水解反应 | |
| D. | 明矾可以用于自来水的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
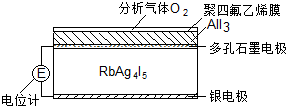 固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及| A. | 4AlI3+3O2=2Al2O3+6I2 | B. | I2+2Ag++2e-=2AgI | ||
| C. | Ag-e-=Ag+ | D. | I2+2Rb++2e-=2RbI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com