(2011?郑州二模)工业上常用铁质容器盛装冷浓硫酸.某学习小组为研究铁质材料与热浓硫酸的反应,设计了以下探究活动:称取铁钉(碳素钢)6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液M并收集到气体N.
(1)该小组通过认真分析,认为M溶液中既含有Fe
3+,也可能含有Fe
2+.若确认溶液中有无Fe
2+,应加入的试剂是
d
d
(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.NaOH溶液 d.酸性KMnO
4溶液
(2)取320mL(标准状况)气体N通入足量溴水中,然后加入足量BaCl
2溶液,经过
过滤
过滤
、
洗涤
洗涤
(填操作名称)、干燥后,得到固体2.33g.气体N与溴水反应的化学方程式为
SO2+Br2+2H2O=H2SO4+2HBr
SO2+Br2+2H2O=H2SO4+2HBr
,计算推知气体N中SO
2的体积分数为
70%
70%
.
(3)该小组通过对铁钉的成分和SO
2体积分数的分析,认为气体N中还可能含有H
2和另外一种气体Q.你认为Q应该是
CO2
CO2
,理由是
C+2H
2SO
4(浓)

2SO
2↑+CO
2↑+2H
2O
C+2H
2SO
4(浓)

2SO
2↑+CO
2↑+2H
2O
(用化学方程式表示).
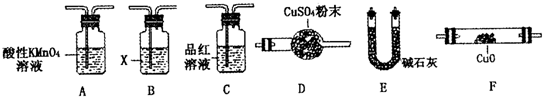
(4)取一定量N,利用下列仪器设计一个能同时检验N中含有H
2和气体Q的装置(夹持仪器、橡胶管和加热装置省略),仪器的连接顺序是
A-C-B-E-F-D(或A-C-B-E-F-D-E)
A-C-B-E-F-D(或A-C-B-E-F-D-E)
(填字母),其中A的作用是
除去N中的SO2
除去N中的SO2
,B中试剂X的化学式是
Ca(OH)2或Ba(OH)2
Ca(OH)2或Ba(OH)2
.

 2SO2↑+CO2↑+2H2O
2SO2↑+CO2↑+2H2O 2SO2↑+CO2↑+2H2O
2SO2↑+CO2↑+2H2O


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案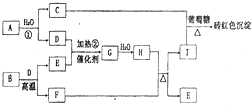 (2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,
(2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,