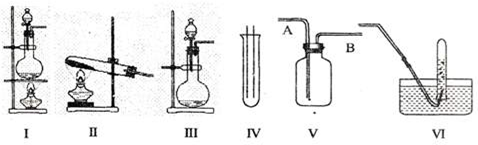
(2010?郑州一模)图Ⅰ、Ⅱ、Ⅲ是常见的气体发生装置;IV、V、VI是气体收集装置,根据要求回答下列问题:
(1)若用MnO
2与浓盐酸反应制取氯气,应选用装置
Ⅰ
Ⅰ
,用方程式表示的制取氯气的反应原理是
MnO
2+4HC1(浓)
MnC1
2+C1
2↑+2H
2O;
MnO
2+4HC1(浓)
MnC1
2+C1
2↑+2H
2O;
.
(2)若用KMnO
4与浓盐酸反应制取氯气,应选用的装置
Ⅲ
Ⅲ
,试完成并配平下列离子方程式:
2
2
MnO
4-+
10
10
C1
-+
16
16
H
+-
2
2
Mn
2++
5
5
C1
2↑+
8H2O
8H2O
.
(3)若选用IV为氯气的收集装置,应该在试管口放置一团棉花,该棉花团应用
氢氧化钠
氢氧化钠
溶液浸湿,其作用是
防止氯气逸出污染空气
防止氯气逸出污染空气
.
(4)若选用V为氯气收集装置,则氯气应从
A
A
口通入.用化学方法检验氯气收集满了的方法是
将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满.
将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满.
.




