
 ,
, ;
;

 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
A、MnO2 与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、铜与稀硝酸反应:Cu+4H++2NO3-═2H2O+Cu2++2NO2↑ | ||||
| C、足量氨水吸收少量二氧化硫气体:NH3?H2O+SO2=NH4++HSO3- | ||||
| D、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只测定它的C、H原子个数比 |
| B、只要证明它完全燃烧后产物只有H2O和CO2 |
| C、只测定其燃烧产物中H2O和CO2的物质的量之比 |
| D、只测定该试样的质量及试样完全燃烧后生成H2O和CO2的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 即使MnO2过量,盐酸也不能全部消耗 |
B、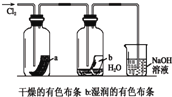 湿润的有色布条能褪色 |
C、 生成棕色的烟 |
D、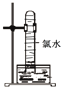 用光照射氯水后液体颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、四个C-H键完全相同 |
| B、CH4的一氯代物只有一种 |
| C、在常温常压下CH2Cl2为液体 |
| D、CH2Cl2只有一种空间结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸铵自发地溶于水 |
| B、2N2O5(g)=4NO2 (g)+O2(g)△H=+156.7kJ/mol |
| C、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)△H=+74.9 kJ/mol |
| D、2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com