
下列关于化学键的说法不正确的是 ( )
A.并不是所有物质都含有化学键
B.只有非金属原子间才能形成共价键
C.单质不可能含有离子键
D.共价化合物中不可能含有离子键
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
用VSEPR模型预测下列分子或离子的立体结构,其中正确的是
A.H2O与BeCl2为V形
B.CS2与SO2为直线形
C.BF3与PCl3为三角锥形
D.SO3与CO为平面三角形
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下期末化学试卷(解析版) 题型:选择题
已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,分别为
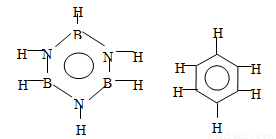
则硼氮苯的二氯取代物(B3N3H4Cl2)的同分异构体的数目为 ( )
A. 2 B. 3 C. 4 D. 5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
具有一个羟基的化合物A 10 g,与乙酸反应生成乙酸某酯11.85 g,并回收了未反应的A 1.3 g,则A的相对分子质量约为( )
A.98 B.116 C.158 D.278
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
在2A+B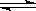 3C+4D反应中,表示该反应速率最快的是 ( )
3C+4D反应中,表示该反应速率最快的是 ( )
A.VA==0.5 mol/(L•s) B. VB==0.3 mol/(L•s)
C.VC==4.8 mol/(L•min) D. VD==1 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高一下期末化学试卷(解析版) 题型:选择题
下列反应中,硝酸只体现氧化性的是 ( )
A.CuO+HNO3 B.Cu+HNO3 C.FeO+HNO3 D.C+HNO3(浓)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高二下期末化学试卷(解析版) 题型:选择题
25℃时,KSP Mg(OH)2 = 5.61 ×10-12 ,KSP MgF2 = 7.42 ×10-11下列说法正确的是
A.25℃时,固体Mg(OH)2在20ml0.01 mol·L-1氨水中的KSP比20mL0.01 mol·L-1NH4Cl溶液中的KSP小
B.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
C.25℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
D.25℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CO2(g)+H2(g) CO(g)+H2O(g)△H2 =+41.2kJ•mol-8平衡常数K2 反应Ⅱ
CO(g)+H2O(g)△H2 =+41.2kJ•mol-8平衡常数K2 反应Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比
(1)合成的甲醇可用于燃料电池的燃料,若电解质为稀烧碱溶液时甲醇燃料电池的正极反应式为________;研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在______极,该电极反应式是________________________________。
(2)从表中实验数据可以分析出,提高CO2转化成CH3OH的选择性的方法有______________。
(3)反应CO(g)+2H2(g) CH3OH(g)的平衡常数K3=____________(用K1和K2表示)。
CH3OH(g)的平衡常数K3=____________(用K1和K2表示)。
(4)在恒压密闭容器中,由CO2和H2进行反应I合成甲醇,在其它条件不变的情况下,探究温度对化学平衡的影响,实验结果如图。
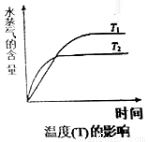
①△H1_________0(填“>”、“<”或“=”)
②有利于提高CO2平衡转化率的措施有___________(填标号)。
A.降低反应温度
B.投料比不变,增加反应物的浓度
C.增大CO2和H2的初始投料比
D.混合气体中掺入一定量惰性气体(不参与反应)
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I。
①充分反应达到平衡后,若CO2转化率为a,则容器的压强与起始压强之比为________(用a表示)。
②若经过3h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为____________(保留三位有效数字);该温度下反应的化学平衡常数K为____________(保留三位有效数字);平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数。写出上述反应压力平衡常数KP为____________(用P0表示,并化简)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一下期末化学试卷(解析版) 题型:选择题
将一定量的SO2和O2充入一个容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g),下列哪个量不再变化时,并不能说明化学反应已达到平衡状态
2SO3(g),下列哪个量不再变化时,并不能说明化学反应已达到平衡状态
A.混合气体的密度
B.混合气体的压强
C.混合气体的平均摩尔质量
D.SO2的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com