
| A、①② | B、③④ | C、①④ | D、③⑤ |
 ,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键;
,氨气分子中氮原子含有孤电子对,但氢原子不含空轨道,所以不能形成配位键; ,无空轨道,无孤电子对,CH4不含有配位键;
,无空轨道,无孤电子对,CH4不含有配位键; 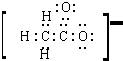 ,不含有配位键;
,不含有配位键;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时铅蓄电池负极的电极反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| B、充电时铅蓄电池阴极的电极反应为;PbSO4+2e-=Pb+SO42- |
| C、用铅蓄电池来电解CuSO4溶液,要生成3.2克Cu,电池内部要消耗0.05摩H2SO4 |
| D、铅蓄电池充电时,若要使3.03千克PbSO4转变为Pb和PbO2,需通过20摩电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、手持试管给试管内的物质加热 |
| B、用燃着的酒精灯去点燃另一盏酒精灯 |
| C、用天平称量药品时用手直接拿砝码 |
| D、配制一定物质的量浓度溶液时,取完浓溶液的量筒不需要洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极反应为O2+4e-+2H2O═4OH- |
| B、正极反应为2H2+4OH--4e-═4H2O |
| C、工作时正极区pH升高,负极区pH降低 |
| D、工作时,电池所消耗的化学能全部转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
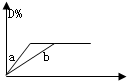 已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0.如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况.若使曲线b变为曲线a,可采取的措施是①增加C的质量 ②升高温度 ③缩小反应容器的容积(加压)④减小B的浓度 ⑤使用适当催化剂( )
已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0.如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况.若使曲线b变为曲线a,可采取的措施是①增加C的质量 ②升高温度 ③缩小反应容器的容积(加压)④减小B的浓度 ⑤使用适当催化剂( )| A、只有⑤ | B、①③ |
| C、③⑤ | D、②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、试剂瓶甲中装浓NaOH溶液,乙中装浓H2SO4 |
| B、分液漏斗中装的试剂可以是盐酸 |
| C、甲中可以盛放KMnO4溶液吸收CO |
| D、甲装置是用于吸收CO2,乙装置是干燥作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AB |
| B、B2C |
| C、A2B2 |
| D、BC2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com