
| A、58.5g NaCl晶体中含有NA个氯化钠分子 |
| B、标准状况下,33.6L CH2O含有的分子数为1.5NA |
| C、78g苯分子中含有的碳碳双键数目为3NA |
| D、含有23g乙醇的水溶液中氢原子数为3NA |
| V |
| Vm |
| V |
| Vm |
| 33.6L |
| 22.4L/mol |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、28g乙烯和28g丙烯中均含有6NA对共用电子对 |
| B、在熔融状态下,1mol NaHSO4完全电离出的阳离子数为2NA |
| C、7.8g Na2O2含有的阴离子数目为0.2NA |
| D、分别处于第二、三周期的两种元素的原子各1 mol,其最外层电子数最多相差8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| B、钠与水的反应:Na+2H2O═Na++2OH-+H2↑ |
| C、铜片跟稀硝酸反应:Cu+NO3-+4H+═Cu2++NO↑+2H2O |
| D、铝片和氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Cu2+、Cl-、SO42- |
| B、Al3+、Na+、Cl-、NO3- |
| C、Ag+、K+、SO42-、Cl- |
| D、K+、Ba2+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、空气:C2H2、CO2、SO2、NO |
| B、氢氧化铁胶体:K+、S2-、Br-、H+ |
| C、0.1mol?L-1 NaAlO2溶液:Al3+、Na+、Cl-、SO42- |
| D、银氨溶液:Na+、K+、NO3-、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeSO4溶液中加入H2O2溶液的反应:Fe2++2H2O2+4H+═Fe3++4H2O |
| B、泡沫灭火器的反应原理为:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
| C、向明矾水溶液中滴加氢氧化钡溶液使SO42-恰好完全沉淀的反应:2Ba2++Al3++2SO42-+3OH-═2BaSO4↓+Al(OH)3↓ |
| D、将溴单质与少量铁加热反应的生成物溶于水,通入足量氯气后发生的反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
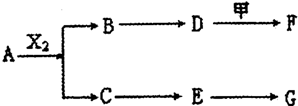
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、46gNO2与46gN2O4中所含原子总数相等,为3NA |
| B、1molNa2O2与足量水充分反应,转移电子总数为2NA |
| C、32gCH4中含有“C-H”键总数为8NA |
| D、标准状况下,11.2L NH3溶于1L水,溶液中含有N原子的微粒总数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径/10-10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com