
| A. | 澄清的石灰水 | B. | 饱和碳酸钠溶液 | C. | 氯化钙溶液 | D. | 硝酸钡溶液 |
分析 A.足量二氧化碳与氢氧化钙反应生成可溶性碳酸氢钙;
B.二氧化碳与碳酸钠溶液反应生成碳酸氢钠,碳酸钠溶解性大于碳酸氢钠;
C.二氧化碳与氯化钙溶液不反应;
D.二氧化碳与硝酸钡不反应.
解答 解:A.足量二氧化碳与氢氧化钙反应生成可溶性碳酸氢钙,不会产生沉淀,故A不选;
B.饱和碳酸钠溶液和二氧化碳反应生成碳酸氢钠,由于碳酸氢钠溶解度比碳酸钠小,则生成沉淀,故B选;
C.二氧化碳与氯化钙溶液不反应,不会产生沉淀,故C不选;
D.二氧化碳与硝酸钡不反应,不会产生沉淀,故D不选;
故选:B.
点评 本题考查了元素及其化合物的性质,熟悉物质性质是解题关键,注意二氧化碳与氢氧化钙反应中反应物用量对反应的影响,注意碳酸钠与碳酸氢钠溶解性区别,题目难度不大.


 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol H2、2molN2 | 4mol H2、4molN2 | 2mol NH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| 平衡时N2的体积分数 | w1 | W2 | W3 |
| 混合气体的密度(g•L-1) | ρ1 | ρ2 | ρ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(ClO)2溶液中通入少量SO2:Ca2++3ClO-+SO2+H2O═CaSO3↓+Cl-+2HClO | |
| B. | 1 mol/L的NaAlO2溶液和2.5 mol/L的盐酸等体积均匀混合:2AlO2-+5H+═Al(OH)3↓+Al3++H2O | |
| C. | 将11.2L标准状况下的氯气通入200mL2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2═2Fe3++4Br2+10Cl- | |
| D. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+═Fe2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q2 | B. | 2Q1=Q2 | C. | Q1<Q2 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氯气及其相关产品在生活、生产中应用广泛.
氯气及其相关产品在生活、生产中应用广泛.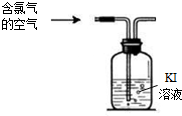
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- | |
| B. | 由水电离产生的c(H+)=10-12mol•L-1的溶液:NH4+、SO42-、HCO3-、Cl- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1014的溶液:Ca2+、Na+、ClO-、NO3- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com