



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Һ�е�c(H��)��1.0��10��13mol��L��1 |
| B��������Һ����ˮ���������c(OH��)��1.0��10��13 mol��L��1 |
| C�����ӵ��ռ���ҺpH��13 |
| D��������Һ�е�c(Mg2��)��5.6��10��10 mol��L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ���������� | Fe2�� | Fe3�� | Zn2�� | Cu2�� |
| ��ʼ����ʱpH | 6.34 | 1.48 | 6.2 | 5.2 |
| ��ȫ����ʱpH | 9.7 | 3.2 | 8.0 | 6.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CuS<Cu(OH)2<CuCO3 | B��CuS>Cu(OH)2>CuCO3 |
| C��Cu(OH)2>CuCO3>CuS | D��Cu(OH)2<CuCO3<CuS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Sr2��(aq)��SO42��(aq)��Ksp��2.5��10��7
Sr2��(aq)��SO42��(aq)��Ksp��2.5��10��7 Sr2��(aq)��CO32��(aq)��Ksp��2.5��10��9
Sr2��(aq)��CO32��(aq)��Ksp��2.5��10��9�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
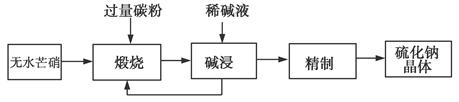
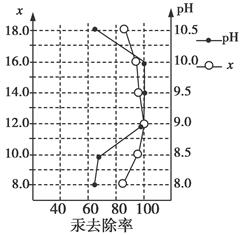
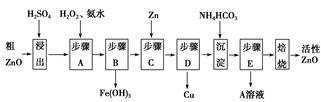
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
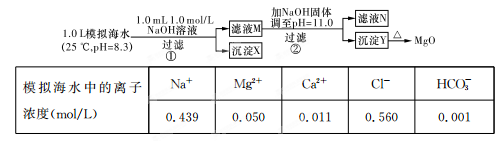
| A��������XΪCaCO3 |
| B����ҺM�д���Mg2+��Ca2+ |
| C����ҺN�д���Mg2+��Ca2+ |
| D�������������Ϊ����4��2 g NaOH���壬������Yֻ��Mg(OH)2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢۢ� | B���ۢܢ٢� | C���ܢۢ٢� | D���ڢ٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ba2��(aq)��SO42-(aq)��Ksp��c(Ba2��)��c(SO42-)�������ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
Ba2��(aq)��SO42-(aq)��Ksp��c(Ba2��)��c(SO42-)�������ܽ�ƽ��������ͼ��ʾ������˵����ȷ����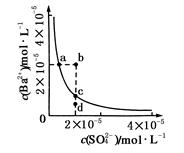
| A��b��ʱc(Ba2��)��c(SO42-)С��Ksp |
| B��a���Ӧ��Ksp����c���Ӧ��Ksp |
| C����ˮϡ�Ϳ���ʹ��Һ��b��䵽c�� |
| D������������Na2SO4������ʹ��Һ��a��䵽c�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com