某研究性学习小组欲探究SO
2能否与BaCl
2溶液反应生成BaSO
3沉淀.查阅资料得知常温下BaSO
3的K
SP为5.48×10
-7,饱和亚硫酸中c(SO
)=6.3×10
-8mol
-1.
(1)将0.1mol?L
-1的BaCl
2溶液滴入饱和亚硫酸中,
(填“能”或“不能”)生成BaSO
3沉淀,原因是
(请写出必要的推断过程).
(2)浓硫酸的沸点为338℃,酒精灯火焰的温度为400-500℃,甲同学用装置Ⅰ进行实验,发现BaCl
2溶液中出现白色沉淀,且白色沉淀不溶于盐酸.
①写出加热试管中发生反应的化学方程式:
②白色沉淀的化学式是
,请用离子方程式表示生成该白色沉淀的可能原因
(3)乙同学认为甲同学的装置不完善,设计了改进装置Ⅱ进行实验(夹持装置和A中加热装置已略,气密性已检验).
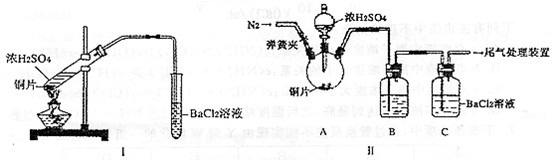
①打开弹簧夹,通入N
2一段时间后关闭弹簧夹
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成.操作①的目的是
,洗气瓶B中的试剂是
.
(4)丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,也产生不溶于盐酸的白色沉淀,丙滴加的试剂可能是
.
A.NaOH 溶液 B.Na[Al(OH)
4]溶液 C.H
2O
2 溶液 D.酸性 KMnO
4 溶液.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案