
A、 检查容量瓶是否漏水 |
B、 给液体加热 |
C、 称量 |
D、 过滤 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |


科目:高中化学 来源: 题型:
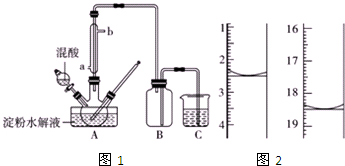 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNa被完全氧化为Na2O2,失去的电子数为2NA |
| B、常温常压下,16gO3气体含有氧原子数为NA |
| C、常温常压下,22.4LCO2 含有分子数为NA |
| D、18g D2O所含有电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1.0×10-14 | α | 1.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
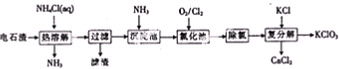
查看答案和解析>>
科目:高中化学 来源: 题型:
| 结构 | 分子中只含有一个苯环,苯环上只有一个取代基且无支链,核磁共振氢谱图中有六个吸收峰,峰面积比为1:2:2:1:1:3 |
| 性质 | ①能使溴水因发生化学反应而褪色②在NaOH溶液中易发生水解反应生成具有剧毒的醇类物质 |
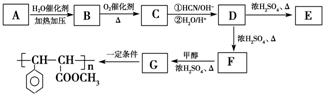
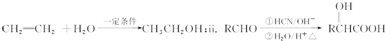
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com