
| A. | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液中有Na+,无K+ | |
| B. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| C. | 进行钠的焰色反应实验,可用到的实验用品有:铂丝、氯化钠溶液、稀盐酸 | |
| D. | 焰色反应是某些金属单质具有的性质 |
分析 A.钠元素的黄色火焰可以覆盖钾元素的紫色火焰;
B.用稀盐酸洗涤并灼烧铂丝后,再进行焰色反应;
C.焰色反应时用盐酸洗涤铂丝,可用灼烧氯化钠的方法观察钠的焰色反应现象;
D.焰色反应是某些金属元素具有的性质.
解答 解:A.钠元素的黄色火焰可以覆盖钾元素的紫色火焰,用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液中有Na+,可能有K+,故A错误;
B.用稀盐酸洗涤并灼烧铂丝后,再进行焰色反应,故B错误;
C.焰色反应时用盐酸洗涤铂丝,用铂丝蘸取氯化钠溶液灼烧,观察钠元素的焰色反应现象,故C正确;
D.焰色反应是某些金属元素具有的性质,包括单质、离子等,故D错误;
故选C.
点评 本题考查焰色反应,侧重于学生的分析能力和实验能力的考查,为高频考点,注意K元素的焰色反应要透过蓝色的钴玻璃片观察,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2SO4溶液可以使蛋白质变性 | |
| B. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| C. | 从海带中提取碘单质的过程涉及氧化还原反应 | |
| D. | 镀锌铁桶镀层破损后铁仍不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
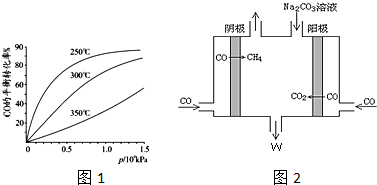
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
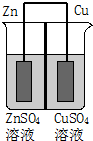 如图为一原电池示意图,在原电池两极之间设有隔膜,离子可以自由通过.则下列说法不正确的是( )
如图为一原电池示意图,在原电池两极之间设有隔膜,离子可以自由通过.则下列说法不正确的是( )| A. | Zn2+通过隔膜从负极区向正极区移动 | |
| B. | 电子由Cu极通过导线流向Zn极 | |
| C. | 一段时间后ZnSO4溶液浓度增大CuSO4溶液浓度减小 | |
| D. | Cu2+与Zn2+物质的量之和保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
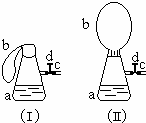 如图(Ⅰ)中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气).将图Ⅰ的装置在托盘天平上称量,质量为W1克.根据实验现象填写下列空白:
如图(Ⅰ)中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气).将图Ⅰ的装置在托盘天平上称量,质量为W1克.根据实验现象填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Q>W>Z | |
| B. | Q的氢化物的水溶液一定具有强酸性 | |
| C. | X、Y、Q可同时存在同一离子化合物中 | |
| D. | 单质的沸点:W>Q>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
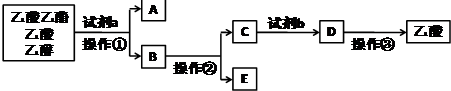
| A. | 操作①用到的玻璃仪器主要有分液漏斗、烧杯 | |
| B. | 工业制备无水E物质的方法是在E中加生石灰后进行操作② | |
| C. | 试剂b可用硫酸 | |
| D. | 操作③用到的仪器和用品主要有漏斗、烧杯、玻璃棒、滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
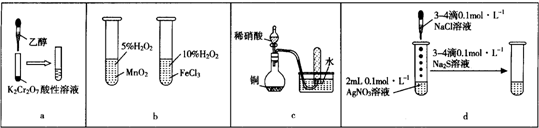
| A. | a图示装置,滴加乙醇试管中橙色溶液变为绿色,乙醇发生消去反应生成乙酸 | |
| B. | b图示装置,右边试管中产生气泡迅速,说明氯化铁的催化效果比二氧化锰好 | |
| C. | c图示装置,根据试管中收集到无色气体,验证铜与稀硝酸的反应产物是NO | |
| D. | d图示装置,试管中先有白色沉淀、后有黑色沉淀,不能验证AgCl的溶解度大于Ag2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com