
NA表示阿伏加德罗常数,下列说法正确的是( )
A.在常温常压下,11.2 LN2含有的分子数为0.5 NA
B.在常温常压下,1molNe含有的原子数为NA
C.71gCl2所含原子数为NA
D.在同温、同压下,相同体积的任何气体单质所含的原子数相同
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年广东省高一上学期第一次月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的有几个( )
①在常温常压下,1mol氦气含有原子数为2NA
②0.5molO2和0.5molO3的混合物所含有的氧原子个数为2.5NA
③常温常压下,18 g H2O中含有的原子总数为3NA
④常温常压下,2.24 LCO和CO2混合气体中含有的碳原子数目为0.1NA
⑤含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol·L-1
⑥1.00 mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
⑦1 mol·L-1 NaCl溶液含有NA个Na+
⑧常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
⑨13.5g Al与足量盐酸反应生成H2的分子数为NA
⑩标准状况下,2.24LCH4所含电子数为NA
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式,不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融)  Mg + Cl2↑[
Mg + Cl2↑[
B.向Ca(ClO)2溶液中通入少量CO2:Ca2+ + 2ClO-+H2O+CO2 == 2HClO +CaCO3↓
C.用CaSO4治理盐碱地:CaSO4(s) + Na2CO3(aq) == CaCO3(s) + Na2SO4(aq)
D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72- + Fe2+ + 14H+ == 2Cr3+ + Fe3+ + 7H2O
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期入学考试化学试卷(解析版) 题型:选择题
N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)  4NO2(g) + O2(g) △H >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g) + O2(g) △H >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是( )
A.500s内NO2的生成速率为2.96×10-3mol·L-1·s-1
B.T1温度下该反应平衡时N2O5的转化率为29.6%
C.达到平衡后,其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)﹤5.00mol/L
D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期开学考试化学试卷(解析版) 题型:实验题
锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌.某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:
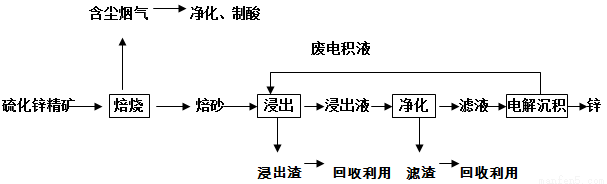
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为_____________;
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的_____________操作。
(3)浸出液“净化”过程中加入的主要物质为_____________,其作用是____________________________。
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气体是_____________。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生的主要反应的离子方程式为______________________。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.凡经加热而发生的化学反应都是吸热反应
B.干冰升华时,二氧化碳分子中的共价键不发生断裂
C.C(石墨,s)=C(金刚石,s),反应中既没有电子得失也没有能量变化
D.伴有能量变化的物质变化,都是化学变化
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列递变情况中,正确的是( )
A. Na、Mg、Al原子的最外层电子数依次减少
B. Si、P、S元素的最高正价依次降低
C. C、N、O的原子半径依次减小
D. Li、Na、K的金属性依次减弱
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期开学考试化学试卷(解析版) 题型:实验题
二甲酸钾是一种白色晶体,商品名为弗米(Formil),是一种能替代抗生素的促生长剂,化学式为KH(HCOO)2,具有吸湿性,易溶于水。
二甲酸钾的生产工艺流程如下:

(1)写出甲酸和碳酸钾生产二甲酸钾的化学方程式: 。
(2)测定某弗米产品纯度的实验方法如下:
称取该弗米产品2.5g,将其全部溶解在水中,配制成250mL未知浓度的溶液,取出25.00mL于锥形瓶中,再滴加2~3滴指示剂,用0.10mol·L-1的NaOH溶液滴定至终点,消耗NaOH溶液的体积为18.50mL。
①加入的指示剂是 (选填“甲基橙”、“石蕊”或“酚酞”),用NaOH溶液滴定至终点的现象是 。
②上述弗米产品中二甲酸钾的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期8月月考化学试卷(解析版) 题型:选择题
下列各表述与示意图一致的是( )
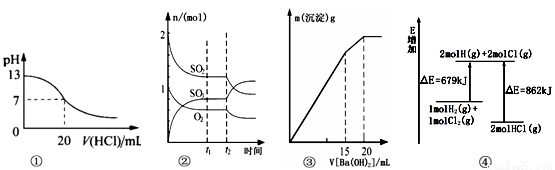
A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线
B.图②表示一定条件下进行的反应2SO2(g) + O2(g) 2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积
2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积
C.图③表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全
D.图④表示化学反应H2(g)+C12(g)== 2HCl(g)的能量变化,则该反应的反应热△H=﹢183 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com