
| A. | I2>Cl2>FeCl3 | B. | FeCl3>Cl2>I2 | C. | Cl2>I2>FeCl3 | D. | Cl2>FeCl3>I2 |
分析 根据反应方程式进行比较:氧化剂+还原剂=还原产物+氧化产物 氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物.
解答 解:根据①反应可知氧化剂为FeCl3、还原剂为KI、还原产物为FeCl2、氧化产物为I2,所以氧化性:FeCl3>I2,还原性为:
KI>FeCl2.根据②可知,氧化剂Cl2、氧化产物为FeCl3、还原剂FeCl2、还原产物为2FeCl3,所以氧化性:Cl2>FeCl3,还原性为:FeCl2>2FeCl3.
故氧化性顺序为:Cl2>FeCl3>I2,故选D.
点评 本题考察了根据方程式来比较氧化性和还原性.解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
深海中存在可燃冰(CH4•nH2O固体).已知:CH4•nH2O(s) 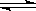 CH4(g)+nH2O(l)﹣Q(Q>0)深海中能够存在可燃冰,是因为深海具有以下条件中的( )
CH4(g)+nH2O(l)﹣Q(Q>0)深海中能够存在可燃冰,是因为深海具有以下条件中的( )
A.低温高压 B.高温低压 C.低温低压 D.高温高压
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol•L-1Na2SO4溶液中Na+个数为2NA | |
| B. | 18g水含有电子数为10NA | |
| C. | 标准状况下,22.4LH2约含有2NA个H | |
| D. | 11.2LH2一定含有NA个H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol•L-1 | B. | 7.8mol•L-1 | C. | 8mol•L-1 | D. | 1.9mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com