
某课外活动小组用如图所示装置进行实验(电解液足量)。下列说法中错误的是( )
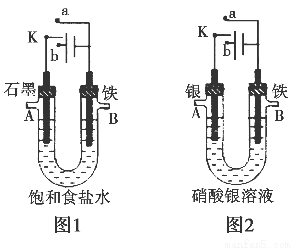
A.图1中,若开始实验时开关K与a连接,则B极的电极反应式为Fe-3e-=Fe3+
B.图1中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度
C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小
D.图2中,若开始实验时开关K与b连接,则A极减少的质量等于B极增加的质量
A
【解析】图1中,若开始实验时开关K与a连接,则形成原电池,电池反应相当于钢铁在中性条件下的吸氧腐蚀,B极的电极反应式应为Fe-2e-=Fe2+,A错。图1中,若开始实验时开关K与b连接,则形成电解池,由于铁棒作阴极,因此电解的总反应式为2NaCl+2H2O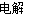 2NaOH+H2↑+Cl2↑,根据元素守恒可知:一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度,B对。图2中,若开始实验时开关K与a连接,则形成原电池,电池总反应式为Fe+2AgNO3=Fe(NO3)2+2Ag,电解液的溶质质量分数变小,C对。图2中,若开始实验时开关K与b连接,相当于电镀装置,根据电镀原理可知D对。
2NaOH+H2↑+Cl2↑,根据元素守恒可知:一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度,B对。图2中,若开始实验时开关K与a连接,则形成原电池,电池总反应式为Fe+2AgNO3=Fe(NO3)2+2Ag,电解液的溶质质量分数变小,C对。图2中,若开始实验时开关K与b连接,相当于电镀装置,根据电镀原理可知D对。
点拨:本题考查电化学知识,意在考查考生对原电池的工作原理和电解原理的掌握程度。


科目:高中化学 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:实验题
Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的物质的量浓度。
(1)在容量瓶的使用方法中,下列操作不正确的是(填字母)________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线
D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(2)现需配制250 mL 0.100 mol·L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250 mL容量瓶、玻璃棒外,还需要________________。
(3)需准确称取Na2S2O3固体的质量为________g。
(4)另取废水50.00 mL,控制适当的酸度,加入足量的K2Cr2O7溶液,得到BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00 mL。已知有关反应的离子方程式为①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;②I2+2S2O32-=2I-+S4O62-。则该工厂废水中Ba2+的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 离子反应、氧化还原反应练习卷(解析版) 题型:填空题
有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32—、SO42—等离子中的几种,为分析其成分,取此溶液分别进行四个实验:
①蘸取溶液进行焰色反应(透过蓝色钴玻璃)显紫色,
②加入盐酸酸化的氯化钡溶液,出现白色沉淀,
③加入过氧化钠固体,产生无色无味的气体和白色沉淀,
④取100 mL该溶液逐滴加入过量的5 mol·L-1氢氧化钠溶液,生成白色沉淀与加入氢氧化钠的量如图:

(1)原溶液中一定不存在的离子:____________________________。
(2)为满足溶液中一定存在的离子要求,一般可溶解两种常见的物质,其化学式为________、________。
x-y=________mol。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电解质溶液练习卷(解析版) 题型:选择题
25℃时,浓度均为1 mol/L的AX、BX、AY、BY四种正盐溶液,AX溶液的pH=7且溶液中c(X-)=1 mol/L,BX溶液的pH=4,BY溶液的pH=6。下列说法正确的是( )
A.AY溶液的pH小于7
B.AY溶液的pH小于BY溶液的pH
C.稀释相同倍数,BX溶液的pH变化小于BY溶液
D.电离平衡常数K(BOH)小于K(HY)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电解质溶液练习卷(解析版) 题型:选择题
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是( )
A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-=Al(OH)3↓
B.加水稀释后,溶液中c(NH4+)·c(OH-)变大
C.用HNO3溶液完全中和后,溶液不显中性
D.其溶液的pH=13
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 电化学原理及其应用练习卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
A.充电时阳极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时OH-向阳极移动
C.放电时每转移3 mol e-正极有1 mol K2FeO4被氧化
D.充电时,电源的正极应与电池的Zn(OH)2极相连
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 物质结构与性质练习卷(解析版) 题型:填空题
Ⅰ.下列有关说法正确的是________。
A.相同类型的离子晶体,晶格能越大,形成的晶体越稳定
B.手性催化剂只催化或者主要催化一种手性分子的合成
C.用金属的电子气理论能合理地解释金属易腐蚀的原因
D.H3O+、NH4Cl和[Ag(NH3)2]+中均存在配位键
Ⅱ.碳及其化合物在自然界中广泛存在。
(1)基态碳原子的价电子排布图可表示为________。
(2)第一电离能:碳原子________(填“>”“<”或“=”)氧原子,原因是__________________________。
(3)冰晶胞中水分子的空间排列方式与金刚石晶胞类似。每个冰晶胞平均占有________个水分子,冰晶胞与金刚石晶胞排列方式相同的原因是__________________________。
(4)C60的晶体中,分子为面心立方堆积,已知晶胞中C60分子间的最短距离为d cm,可计算C60晶体的密度为________g/cm3。
(5)请写出一个反应方程式以表达出反应前碳原子的杂化方式为sp2,反应后变为sp3:________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 物质结构、元素周期律练习卷(解析版) 题型:选择题
11)有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍。下列说法中不正确的是( )
A.W、M的某种单质可作为水处理中的消毒剂
B.电解YW2的熔融物可制得Y和W的单质
C.相同条件下,W的氢化物水溶液酸性比Z弱
D.X、M两种元素形成的一种化合物与水反应可生成M的某种单质
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 有机化学基础练习卷(解析版) 题型:选择题
符合下列条件的烃的一氯代物共有(不考虑立体异构)( )
①分子中碳元素与氢元素的质量之比为21:2;②含一个苯环;③相对分子质量小于150。
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com