
在高温时,
N2与O2可以发生微弱的反应生成NO(用化学方程式表示形成过程,下同):________.NO是一种________色、不溶于水的有毒气体,是大气污染物之一,其性质不稳定,在空气中易被氧化为NO2:________.NO2是一种________色、有刺激性气味的有毒气体,易液化,性质较稳定.NO2能部分自动聚合成无色的N2O4:________,也能与水反应生成硝酸:________.科目:高中化学 来源: 题型:
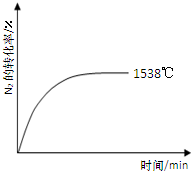 自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 9 |
| 1 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 11.82g |
| 197g/mol |
| 11.82g |
| 197g/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com