

| A、甲池中,Cu极上有气泡放出 |
| B、发现a点附近显红色 |
| C、电子走向Zn→a→b→C2 |
| D、乙池溶液的pH减小 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、葡萄糖的分子式:C6H12O6 |
| B、氯气的电子式:Cl:Cl |
| C、乙醇的结构简式:CH3CH2OH |
D、硫原子的结构示意图: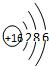 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、属于芳香烃 |
| B、属于卤代烃 |
| C、该有机物有四种官能团 |
| D、该有机物的分子式为C23H21O3NBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、中子数为8的N原子:
| ||
B、硫离子的结构示意图: | ||
| C、H2O2的结构式:H-O-O-H | ||
| D、石英的化学式:Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 固体催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如图所示,已知E为气体单质,能使带火星的木条复燃.
已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如图所示,已知E为气体单质,能使带火星的木条复燃.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com