
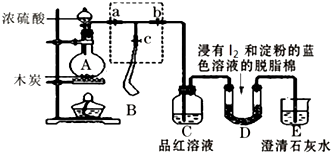
分析 (1)装置图象分析可知A中盛浓硫酸的仪器为分液漏斗;
(2)浓硫酸有强氧化性,能将C氧化为二氧化碳;
(3)二氧化硫能使品红溶液褪色;
(4)根据具体操作可知,要控制气体流速,应先收集气体,然后慢慢挤压气球来控制流速;
(5)进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变时出气口出的是二氧化碳;碘单质能将二氧化硫氧化为硫酸,结合电子守恒计算生成气体体积;
解答 解:(1)装置A中盛放浓硫酸的仪器名称为分液漏斗,
故答案为:分液漏斗;
(2)装置A中浓硫酸有强氧化性,能将C氧化为二氧化碳,反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)二氧化硫具有漂白性,所以C中品红溶液褪色,
故答案为:品红溶液褪色;
(4)气囊B的作用是收集气体,要想控制流速,从虚线框设计来看,应先收集气体,然后再慢慢释放气体,所以正确的操作顺序为:③①②,
故答案为:③①②;
(5)当D装置中进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变时,出气口出的是二氧化碳,碘单质能将二氧化硫氧化为硫酸,反应的化学方程式为:I2+SO2+2H2O=H2SO4+2HI,反应中电子转移2e-发生反应的气体二氧化硫物质的量为1mol,当D中反应发生0.3mol电子转移时,发生反应的气体的物质的量=0.15mol,体积(标准状况)=22.4L/mol×0.15mol=3.36L,
故答案为:进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变;I2+SO2+2H2O=H2SO4+2HI; 3.36.
点评 本题考查了浓硫酸的性质及化学计算,题目难度中等,根据实验目的和装置图考虑操作步骤和试剂的作用及发生反应即可解答,(5)为易错点,注意明确只有出口处脱脂棉蓝色不变时才能说明无二氧化硫,试题培养了学生灵活应用基础知识的能力和化学实验能力.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | 在相同状况下,20mL NH3与60mLO2所含的分子数之比为1:3 | |
| B. | 标准状况下,11.2 L H2O所含的分子数为 NA | |
| C. | 常温常压下,16g O2 与16gO3含有的分子数不相同 | |
| D. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ls22s22p63s23p3 | B. | 1s22s22p3 | C. | 1s22s2sp2 | D. | 1s22s22p63s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤⑦ | B. | ①③⑤④ | C. | ①②③⑤⑥ | D. | ③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 少量SO2气体通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO | |
| D. | Ca(HCO3)2溶液和少量NaOH溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 短周期是指第1、2周期 | B. | 过渡元素全部是金属元素 | ||
| C. | 元素周期表有8个副族 | D. | IA族的元索全部是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐放在水中片刻后消失了 | |
| B. | 食醋洒在大理石台面上产生气泡 | |
| C. | 烧菜用过的铁锅,放置后常出现红棕色斑迹 | |
| D. | 用食醋可以除去水壶中的水垢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com