A������ѡѧ����ѧ�������������
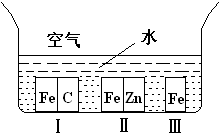
��1������ͼ��ʾ�������ڢ����ֲ�ͬ�Ļ����У�������ʴ�������ɴ�С��˳����
������ţ�
��2�����ȴ�����һ���ƻ�����������ʣ��ڴ���ƽ�����У����ȴ����������ߵ�����ֽ����ԭ�ӣ���ԭ�Ӳ��������йط�Ӧ��
��Cl+O
3��ClO+O
2����O
3��O+O
2����ClO��Cl+O
2���з�Ӧ���ܷ�Ӧʽ��
��
��3��̼�������dz��������ɼ�����Ҫ����Ϊ���ڼ��������²��������壬ʹʳƷ������ɣ���д��̼���������ȷֽ�Ļ�ѧ����ʽ
��
��4��������Դ���ķ�����
��
A������ B������ C���ѷʷ� D��������շ�
B����ѡѧ����ѧ��Ӧԭ������������
�跴Ӧ��Fe��s��+CO
2��g���TFeO��s��+CO��g����ƽ�ⳣ��ΪK
1����Ӧ��Fe��s��+H
2O��g���TFeO��s��+H
2��g����ƽ�ⳣ��K
2���ڲ�ͬ�¶��£�K
1��K
2��ֵ���£�
| �¶� |
K1 |
K2 |
| 973K |
1.47 |
2.38 |
| 1173K |
2.15 |
1.67 |
��1�����ϱ������ƶϣ���Ӧ����
������������š����ȷ�Ӧ����Ӧ����
������������š����ȷ�Ӧ��
��2�����з�Ӧ��CO
2��g��+H
2��g���TCO��g��+H
2O��g��д���÷�Ӧ��ƽ�ⳣ��K
3����ѧ����ʽ��K
3�T
��
��3����д�Ȼ�ѧ����ʽ��
��1mol N
2��g��������O
2��g����Ӧ������NO
2��g��������68KJ������
��
��NH
3��g��ȼ������NO
2��g����H
2O��g������֪
��1��2H
2��g��+O
2��g���T2H
2O��g����H�T-483.6kJ/mol
��2��N
2��g��+2O
2��g���T2NO
2��g����H�T+67.8kJ/mol
1��N
2��g��+3H
2��g���T2NH
3��g����H�T-92.0kJ/mol
NH
3��g��ȼ������NO
2��g����H
2O ��g���Ȼ�ѧ����ʽ��
��

 A������ѡѧ����ѧ�������������
A������ѡѧ����ѧ�������������

 �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�