
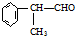 的物质,该物质是一种香料.
的物质,该物质是一种香料.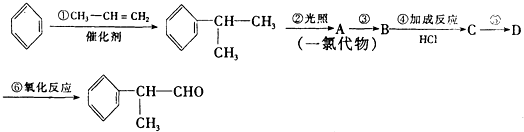
 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2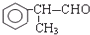 +2H2O.
+2H2O.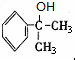 生成
生成 、
、 、
、 .
. 分析 在光照条件下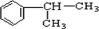 可与氯气发生取代反应生成A
可与氯气发生取代反应生成A ,B能发生加成反应,则A应发生消去反应,B为
,B能发生加成反应,则A应发生消去反应,B为 ,根据产物可知D为
,根据产物可知D为 ,则C为
,则C为 ,以此解答该题.
,以此解答该题.
解答 解:在光照条件下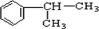 可与氯气发生取代反应生成
可与氯气发生取代反应生成 ,B能发生加成反应,则A应发生消去反应,B为
,B能发生加成反应,则A应发生消去反应,B为 ,根据产物可知D为
,根据产物可知D为 ,则C为
,则C为 .
.
(1)由以上分析可知A为 ,故答案为:
,故答案为: ;
;
(2)由异丙苯的结构可知,反应①为苯与丙烯发生加成反应,反应③为A发生消去反应生成 ,⑤为
,⑤为 发生取代反应生成
发生取代反应生成 ,
,
故答案为:加成反应,消去反应,取代反应或水解反应;
(3)反应⑥的化学方程式为2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2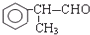 +2H2O,
+2H2O,
故答案为:2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2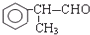 +2H2O;
+2H2O;
(4)A为 ,D为
,D为 ,
,
中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:中间产物A的结构不确定,若直接由A转化为D会有大量副产物 生成,
生成,
故答案为:中间产物A的结构不确定,若直接由A转化为D会有大量副产物 生成;
生成;
(5)①该物质的水溶液遇FeCl3溶液呈紫色,说明含有酚羟基,
②分子中有苯环,且苯环上的一溴代物有两种,则苯环上有2个取代基,且位于对位位置,可能为 ,
,
故答案为: 、
、 、
、 .
.
点评 本题考查有机物的推断,题目难度中等,本题注意可用正逆推结合的方法推断,答题时注意把握题给信息,为解答该题的关键,注意同分异构体的判断.


科目:高中化学 来源: 题型:推断题
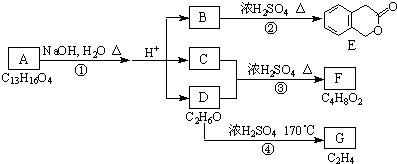
 .反应①的反应类型是水解反应.
.反应①的反应类型是水解反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
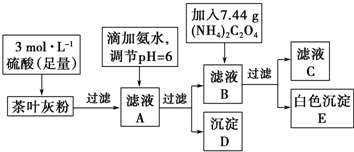
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋清洗茶壶上的水垢:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Fe(SCN)3溶液中滴NaOH溶液:Fe(SCN)3+3OH-═Fe(OH)3↓+3SCN- | |
| C. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| D. | 钠在空气中加热燃烧:4Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$2Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
 .
. .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X、W的最外层电子数均为6 | B. | 最高价氧化物的水化物的碱性:Y>Z | ||
| C. | 简单气态氢化物的稳定性:W>X | D. | Y的单质在X的单质中燃烧生成Y2X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com