
【题目】恒容密闭容器中进行反应mX(g)+nY(g) ![]() qZ(g)ΔH>0,m+n<q达到平衡时,下列说法正确的是 ( )
qZ(g)ΔH>0,m+n<q达到平衡时,下列说法正确的是 ( )
A. 通入稀有气体使压强增大,平衡将正向移动
B. X的逆反应速率是Y的正反应速率的n/m倍
C. 降低温度,混合气体的平均相对分子质量变小
D. 增加X的物质的量,X的转化率降低
【答案】D
【解析】
A.体积不变的条件下,通入与反应无关的气体,不影响反应混合物浓度,速率不变,平衡不动;B.同一反应,不同物质的速率之比等于化学方程式的系数之比;C.该反应正向是放热反应,降温平衡正向移动;反应物、生成物均为气体时,根据质量守恒,气体总质量不变,根据平均分子量计算公式:![]() =
=![]() 进行分析;D. 反应物不止一种时,增加一种反应物的量,会提高另一种物质的转化率;参与反应的该物质增多,但由于自身的总量也在增加,所以自身的转化率反而会降低。
进行分析;D. 反应物不止一种时,增加一种反应物的量,会提高另一种物质的转化率;参与反应的该物质增多,但由于自身的总量也在增加,所以自身的转化率反而会降低。
恒容时通入稀有气体总压增大,反应混合物浓度不变,平衡不动,A错误;速率之比等于化学方程式的系数之比,v(X):v(Y)= m:n,平衡时,X的逆反应速率是Y的正反应速率的m/n倍,B错误;反应正向是放热反应,降温平衡正向进行,反应前后气体体积减小,即气体总物质的量减小,且过程中气体总质量不变,根据![]() =
=![]() ,所以混合气体的相对分子质量增大,C错误; 增加X的物质的量会提高Y的转化率,X自身的转化率降低,D正确;正确选项:D。
,所以混合气体的相对分子质量增大,C错误; 增加X的物质的量会提高Y的转化率,X自身的转化率降低,D正确;正确选项:D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:氯化银、溴化银、硫化银的Ksp分别为1.56×10﹣10、7.7×10﹣13、6.3×10﹣50 , 某溶液中含有浓度均为 0.01mol/L 的Cl﹣、Br﹣、S2﹣ , 向该溶液中逐滴滴加0.01mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序是( )
A.Cl﹣、Br﹣、S2﹣
B.Br﹣、Cl﹣、S2﹣
C.S2﹣、Br﹣、Cl﹣
D.Br﹣、S2﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应. 2R﹣C≡C﹣H ![]() R﹣C≡C﹣C≡C﹣R+H2
R﹣C≡C﹣C≡C﹣R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值.下面是利用Glaser反应制备化合物E的一种合成路线: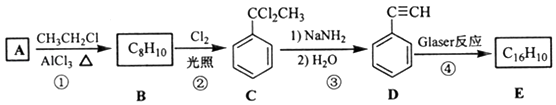
回答下列问题:
(1)B的结构简式为 , D 的化学名称为 .
(2)①和③的反应类型分别为、 .
(3)E的结构简式为 . 用1mol E合成1,4﹣二苯基丁烷,理论上需要消耗氢气mol.
(4)化合物( ![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为 .
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为 .
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式 , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用.下面化学反应不符合绿色化学理念的是( )
A.消除硫酸厂尾气排放:SO2+2NH3+H2O═(NH4)2SO3
B.治理汽车尾气中NO和CO,可利用催化装置将NO与CO转化成CO2和N2
C.制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
D.制CuSO4:2Cu+O2 ![]() 2CuO CuO+H2SO4═CuSO4+H2O
2CuO CuO+H2SO4═CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I是重要有机中间体,其合成路线(部分反应条件已略去)如下图所示:

已知:
R — CN![]() R — COOH
R — COOH
回答下列问题:
(1)A的结构简式是______________。
(2)B中含有的官能团是______________。
(3)D是一种合成高分子,它的结构简式是______________。
(4)I发生缩聚反应的化学方程式是______________。
(5)G→H的反应类型是______________。
(6)E→F反应的化学方程式是______________。
(7)下列说法正确的是________。
①物质I能发生消去反应
②F→G过程产生的副产物 物质G互为同分异构体
物质G互为同分异构体
③B、D均存在顺反异构
(8)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选)________。(合成路线常用的表示方式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素最外层电子数与原子序数的关系图. 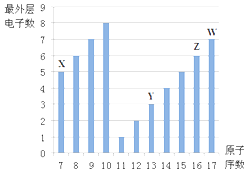
请回答下列问题:
(1)画出Z的原子结构示意图 .
(2)原子半径:YZ(填“>”、“<”).
(3)Y的最高价氧化物的水化物与氢氧化钠溶液反应的化学方程式为 .
(4)X的最高价氧化物的水化物的化学式为 .
(5)画出W的氢化物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图所示装置进行实验,并回答下列问题:

(1)判断装置A和B的能量转化形式:A池为______________,B池为_________________。
(2)锌电极发生 _________反应;铜极发生__________________________反应;石墨棒C1为____极,电极反应式为_________;石墨棒C2附近发生的实验现象___________。
(3)当C2极析出44.8 L气体(标准状况下),锌的质量变化为(增加或减少)________g。CuSO4溶液的质量变化为(增加或减少)________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com