
无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
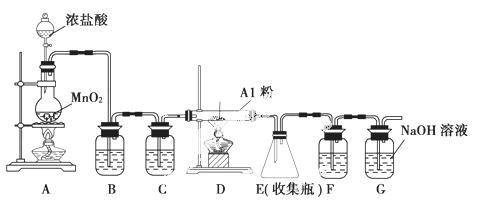
装置B中盛放饱和NaCl溶液,该装置的主要作用是________。F中试剂的作用是________。用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为________。
科目:高中化学 来源: 题型:
有①CH3COOH;②HCl;③H2SO4 三种酸。
(1)CH3COOH溶液中,其电离平衡常数表达式为K = _________________
(2)0.1 mol/L的三种酸溶液,c(H+)由大到小的排列顺序是 (填序号)。
(3)体积相同、c(H+)相同的三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是 (填序号)。
(4)将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为___________;
(5)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
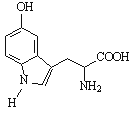
5—羟色胺对人体睡眠具有调节作用,其结构简式如右图所示。下列有关5—羟色胺说法错误的是
A.该有机物分子式为C11H12N2O3
B.该有机物分子中所有原子不可能共平面
C.分子中含有1个手性碳原子
D.1mol该物质最多可与4molH2或1molBr2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理知识回答下列有关碳和碳的化合物的问题:
(1)汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应△H<0). 在2 L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
|
T/℃ n/mol | NO | CO | E | F |
| 初始 | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
①请结合上表数据,写出NO与CO反应的化学方程式 .
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2,根据表中数据计算K1= 。根据表中数据判断,温度T1和T2的关系是(填序号)__________。
A.T1>T2B.T1<T2 C.T1=T2 D.无法比较
(2)反应生成的气体E经常用氢氧化钠来吸收,现有0.4molE,若用200mL 3mol/L NaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为: .
(3)已知CH4、H2和CO的燃烧热分别为890.3kJ/mol,285.8 kJ/mol和283.0 kJ/mol,工业上利用天然气(主要成分是CH4)与CO2进行高温重整制备CO和H2,写出该反应的热化学方程式: .
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质,CO为负极燃气,空气与CO2 的混合气为正极助燃气,制得在 650 ℃下工作的燃料电池,写出其负极和正极电极反应方程式:负极: ;正极: .
查看答案和解析>>
科目:高中化学 来源: 题型:
诺贝尔物理学奖授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是( )
A.二氧化硅是H2SiO3的酸酐,因此能与水反应
B.用二氧化硅制取单质硅时,当生成2.24 L(标况)气体时,得到2.8 g硅
C.6 g的二氧化硅中含有0.2 mol的共价键
D.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组为探究铜与浓硫酸的反应,用如图所示装置进行有关实验。实验中甲同学将a g铜片和12 mL 8 mol·L-1浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。

请回答下列问题:
(1)请写出Cu与浓H2SO4反应的化学方程式:____________。
(2)装置D内盛品红溶液,当C中气体集满后,D中有可能观察到的现象是______________________________________________。
实验装置D有可能造成环境污染,试用最简单的方法加以解决(实验用品自选)__________________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B装置中的现象是____________________________________。
(4)F中应放置的液体是________(填序号)。
A.饱和Na2SO3溶液
B.酸性KMnO4溶液
C.浓溴水
D.饱和NaHSO3溶液
(5)为什么有一定量的余酸,但未能使Cu完全溶解,你认为原因是_____________________________________________________。
(6)下列足量药品能够用来证明反应结束后的烧瓶中确有余酸的是________(填序号)。
A.铁粉 B.BaCl2溶液
C.Ag D.Na2CO3溶液
(7)甲同学向A中反应后的溶液中通入一种气 体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是________(填名称),反应方程式是_____________________________________________。
体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是________(填名称),反应方程式是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用相关化学知识进行 判断,下列结论错误的是
判断,下列结论错误的是
A.某吸热反应能自发进行,因此该反应是熵增反应
B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C.可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施不合理的是
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用 Na2S作沉淀剂,除去废水中的Cu2+和Hg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列实验事实与硝酸性质不相对应的一组是( )
A.浓硝酸使紫色石蕊试液先变红后退色——酸性和强氧化性
B.不能用稀硝酸与锌反应制取氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液红色退去——强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com