
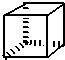
 “立方烷”是新合成的一种烃,其分子为正立方体结构,其结构如图所示:
“立方烷”是新合成的一种烃,其分子为正立方体结构,其结构如图所示: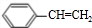 ;这种芳香烃异构体与单体ACH2=C(CH3)CC(CH3)=CH2(写结构简式)可合成具有
;这种芳香烃异构体与单体ACH2=C(CH3)CC(CH3)=CH2(写结构简式)可合成具有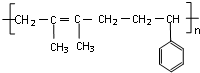
分析 (1)根据碳原子的价键理论和键线式的特点来书写化学式,烃的二氯代物的同分异构体可以采用固定一个氯原子的方法来寻找;
(2)立方烷(C8H8)属于芳香烃的同分异构体,结构中含有1个苯环,不饱和度为$\frac{8×2+2-8}{2}$=5,故侧链为-CH=CH2; 链节主链中含有C=C双键,有6个C原子,为烯烃与二烯烃加聚产物,其单体为苯乙烯与CH2=C(CH3)CH=CH2;
链节主链中含有C=C双键,有6个C原子,为烯烃与二烯烃加聚产物,其单体为苯乙烯与CH2=C(CH3)CH=CH2;
(3)A为CH2=C(CH3)CC(CH3)=CH2,和溴水反应的一种生成物存在顺反异构,应为1,4加成,以此判断产物.
解答 解:(1)该烃的每一个碳原子均和三个碳原子成键,剩余的一个键是和氢原子成键,则立方烷的分子式为:C8H8,立方烷二氯代物的同分异构体分别是:一条棱、面对角线、体对角线上的两个氢原子被氯原子代替,所以立方烷二氯代物的同分异构体有3种,
故答案为:C8H8;3;
(2)立方烷(C8H8)属于芳香烃的同分异构体,结构中含有1个苯环,不饱和度为$\frac{8×2+2-8}{2}$=5,故侧链为-CH=CH2,符合条件同分异构体为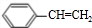 .
. 链节主链中含有C=C双键,有6个C原子,为烯烃与二烯烃加聚产物,其单体为苯乙烯与CH2=C(CH3)CC(CH3)=CH2.
链节主链中含有C=C双键,有6个C原子,为烯烃与二烯烃加聚产物,其单体为苯乙烯与CH2=C(CH3)CC(CH3)=CH2.
故答案为: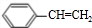 ;CH2=C(CH3)CC(CH3)=CH2;
;CH2=C(CH3)CC(CH3)=CH2;
(3)A为CH2=C(CH3)CC(CH3)=CH2,和溴水反应的一种生成物存在顺反异构,其反应的化学方程式为CH2=C(CH3)CC(CH3)=CH2+Br2→CH2BrC(CH3)=CC(CH3)CH2Br,
故答案为:CH2=C(CH3)CC(CH3)=CH2+Br2→CH2BrC(CH3)=CC(CH3)CH2Br.
点评 本题考查有机物的结构和性质,为高频考点,题目侧重考查同分异构体书写、加成反应等,难度中等,注意把握有机物的加聚反应和顺反异构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 加压 | B. | 减压 | C. | 降温 | D. | 减少E的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ | B. | SO42- | C. | S 2- | D. | NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| B. | 在组装蒸馏装置时,温度计的水银球应伸入液面下 | |
| C. | 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水 | |
| D. | 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温才过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20 | B. | 15 | C. | 25 | D. | 16 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 微热 | B. | 加入适量氧化铜 | ||
| C. | 加入少量硫酸铜溶液 | D. | 加水 | ||
| E. | 加入少量氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
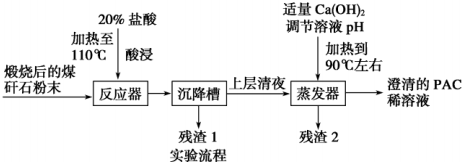
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com