
【题目】下列说法正确的是
A.摩尔是一种物理量B.标准状况下的气体摩尔体积约为22.4 L
C.CO2的摩尔质量是44gD.500mL0.1mol/L AlCl3溶液中Cl-的浓度为0.3mol/L
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】复分解反应是中学化学中常见的一种反应类型。复分解反应中,元素的化合价都没发生变化,都不属氧化还原反应。
(1)复分解反应存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐。已知相同物质的量浓度的溶液,pH大小关系是pH(Na2CO3)>pH(NaClO)>pH(NaHCO3)>pH(NaHS O3)。
①写出向NaClO溶液中通入少量CO2的化学方程式______________________。
②将混有CO2气体的SO2气体,通入NaHSO3饱和溶液,___________(填“能”或“不能”)除去CO2气体。
(2)复分解反应从形式上看,是一种相互交换成分的反应,在有机反应中,也存在类似形式的反应——“烯烃的复分解”反应。

如果用重氢(D)标记过的烯烃CD3CD![]() CDCD3和烃CH3CH
CDCD3和烃CH3CH![]() CHCH3进行反应,其化学方程式是______________________。
CHCH3进行反应,其化学方程式是______________________。
(3)复分解反应的发生还遵循向生成沉淀、气体、难电离物质的方向进行。
①甲同学认为CuSO4+H2S![]() H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
H2SO4+CuS↓不能发生,因为该反应违背了“较强酸制较弱酸”的原则。请你判断甲同学的观点是否正确,并做出解释:________________。
②乙同学认为,BaSO3可溶于酸,SO2通入Ba(NO3)2溶液中不发生化学反应,但经过实验探究发现,有白色沉淀生成,请你写出相关反应的离子方程式_____________。
(4)电解是一种在通电作用下的氧化还原反应。用电解法可将某工业废水中的CN-转变为N2,装置如上图所示。电解过程中,阴极区电解质溶液的pH将_____________(填“增大”“减小”或“不变”)。阳极的电极反应式为______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲除去甲烷气体中混有的乙烯得到纯净的甲烷,最好依次通过盛有( )试剂的装置.
A.澄清石灰水、浓H2SO4
B.酸性KMnO4溶液、浓H2SO4
C.溴水、浓H2SO4
D.CCl4、碱石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期三种元素X、Y、Z,原子序数依次递增,它们的最高价氧化物的水化物皆为强酸,下列说法不正确的是( )
A. Y 在自然界中存在游离态 B. 最高正价:X > Y > Z
C. Y 气态氢化物溶于水呈酸性 D. 非金属性:Y < Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在 5L 的密闭容器中发生如下反应:N2 (g)+3H2 (g)2NH3(g),起初充入的 3.0mol N2 和 6.0mol H2 , 5 分钟后达到平衡,此时容器内压强是开始时的 ![]() ,问:
,问:
(1)氢气的平衡转化率为;
(2)用氨气表示 5min 内的反应速率为
(3)若要使氮气和氢气的平衡转化率相等,起始投料要求 n(H2 ):n(N2 )为
(4)以下措施能加快反应速率的是
A.缩小体积,使压强增大
B.恒温恒容充入 He 使压强增大
C.恒温恒压充入 He
D.平衡后加入催化剂
(5)如果利用此反应设计成原电池,并用稀硫酸做电解液,分别写出正、负极的电极反应 式:、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用萃取法从碘水中分离碘,所用萃取剂应具有的性质是( ) ①不和碘或水起化学反应 ②能溶于水 ③不溶于水 ④应是极性溶剂 ⑤应是非极性溶剂.
A.①②⑤
B.②③④
C.①③⑤
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.所有的电子在同一区域里运动
B.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
C.处于最低能量的原子叫基态原子
D.同一原子中,1s、2s、3s所能容纳的电子数越来越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是前20号元素中的部分元素的一些数据:
A | B | C | D | E | F | G | H | I | J | |
原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
试回答下列问题:
(1)以上10种元素电负性最大的是_____(填元素符号)。比元素B原子序数大7的元素在元素周期表中的位置:第_____周期,第_____族,其基态原子的核外电子排布式是________。
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)__________。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成________个σ键,________个π键。
(4)I与氢元素形成的10电子分子X的空间构型为________;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为________,其中X与Cu2+之间以_____________键结合。
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a._________________________________。
b._________________________________。
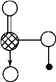
(6) 如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为_________,若晶胞边长为a cm,则晶体的密度为_______________(用含a、NA的代数式表示)(g/mL)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com