
һ���¶��£����ݻ��̶����ܱ������н��еĿ��淴Ӧ��2NO2 2NO��O2���ﵽƽ��ı�־�ǣ� ��
2NO��O2���ﵽƽ��ı�־�ǣ� ��
����ͬʱ���ڣ���������������Ϊn mol��L��1��s��1��NO2����������Ϊ2n mol��L��1��s��1��
�ڵ�λʱ��������n mol O2��ͬʱ����2n mol��NO
�ۻ���������ɫ���ٱ仯��
�ܻ��������ܶȱ��ֲ��䡡
�ݻ�������ƽ����Է����������ٸı䡡
��ѹǿ����ʱ��仯���仯
A���٢ۢݢ� B���ڢۢ�
C���٢ۢ� D���٢ڢۢܢݢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�鷽���ܴﵽʵ��Ŀ�ĵ���
A���õ�����Һ������Һ���Ƿ���ڵⵥ�� B���÷�Һ©������ˮ���Ҵ��Ļ����
C�����Ȼ�����Һ����̼������Һ����������Һ D���������ſ������ռ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺
�ٽ�2.3 g���л�����ȫȼ�գ�����0.1 mol CO2��2.7 g H2O��
���������Dzⶨ����Է���������������ͼ��ʾ������ͼ��
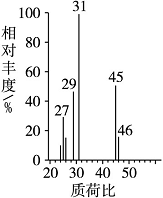
���ú˴Ź����Ǵ����û�����õ�����ͼ��ʾ��ͼ��ͼ������������֮����1��2��3��
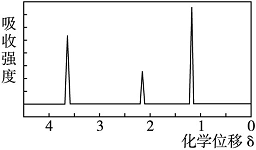
�Իش��������⡣
(1)�л���A����Է���������________��
(2)д���л���A�Ľṹ��ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö��Ե缫���ij��Һʱ����������ֻ��H2��O2���ɣ�����һ��ʱ��������ǰ���¶ȱ仯���Բ��ƣ������й���Һ������ȷ����
�ٸ���Һ��pH��������ڸ���Һ��pH���ܼ�С�۸���Һ��pH���ܲ���ܸ���Һ��Ũ�ȿ�������ݸ���Һ��Ũ�ȿ��ܲ������Һ��Ũ�ȿ��ܼ�С�� ��
A���٢ڢۢܢݡ������� B��ֻ�Т٢ڢۢܡ�������
C��ֻ�Т٢ۢݡ����� D���٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
COCl2 ��g�� CO��g��+ Cl2��g�� ��H>0,����Ӧ�ﵽƽ��ʱ�����д�ʩ�����¢ں���ͨ��������������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ��ǣ� ��
CO��g��+ Cl2��g�� ��H>0,����Ӧ�ﵽƽ��ʱ�����д�ʩ�����¢ں���ͨ��������������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ��ǣ� ��
A. �٢ڢ� B. �٢ܢ� C. �ڢۢ� D. �ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
800��ʱ����2L�ܱ������з���2NO(g)��O2(g)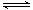 2NO2(g)�����n(NO)��ʱ��ı仯���±���
2NO2(g)�����n(NO)��ʱ��ı仯���±���
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
��1����O2��ʾ2sʱ�÷�Ӧ��ƽ������v ��__________________��
��2��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��__________________________ ___ ����֪��K(800��)��K(850��)���÷�Ӧ��__________������ȡ����ȡ�����Ӧ��
��3����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����___________��
A��v(NO2)=2v(O2) B��������ѹǿ���ֲ���
C��v��(NO)��2v��(O2) D��������������ܶȱ��ֲ���
��4�����в����У���ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����_______��
A����ʱ�����NO2���� B���ʵ������¶�
C������O2��Ũ�� D��ѡ���Ч�Ĵ���
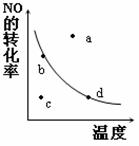
��5����ͼ�е����߱�ʾ������������һ��ʱ����Ӧ��2NO (g)+O2(g) 2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ��ͼ�б���a��b��c��d�ĵ㣬���б�ʾδ�ﵽƽ��״̬����v(��)>v(��)�ĵ��� ��
2NO2(g)��NO��ƽ��ת�������¶ȵĹ�ϵ��ͼ�б���a��b��c��d�ĵ㣬���б�ʾδ�ﵽƽ��״̬����v(��)>v(��)�ĵ��� ��
A��a�� B��b��
C��c�� D��d��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2 mol A��2 mol B�����2 L���ܱ������з�Ӧ��2A(g)��3B(g) 2C(g)��zD(g)
2C(g)��zD(g)
��2 s��A��ת����Ϊ50%�����v(D)��0.25 mol��L��1��s��1�������ƶ���ȷ���ǣ� ��
A��v(C)��0.2 mol��L��1��s��1 B��z��3
C��B��ת����Ϊ25% D��C���������Ϊ28.6%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ�����������ȷ����(����)��
A����ˮ�Լ��ԣ�NH3��H2O === NH4�� �� OH��
B������������Һ�����ԣ�NaHSO4 === Na�� �� H�� �� SO42��
C��Na2S��Һ�Լ��ԣ�S2�� �� 2H2O  H2S �� 2OH��
H2S �� 2OH��
D��AlCl3��Һ�����ԣ�Al3�� �� 3H2O Al(OH)3�� �� 3H��
Al(OH)3�� �� 3H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������Ͷ�뵽�����У��������������ɵ��ǣ� ��
A��Na B��Na2O C��Na2O2 D��Na2CO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com