
| A. | 糖类在一定条件下可以水解生成乙醇和二氧化碳 | |
| B. | 检验淀粉在稀硫酸催化条件下水解产物的方法:取适量水解液于试管中,加入少量新制Cu(OH)2溶液,加热,观察是否出现砖红色沉淀 | |
| C. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 | |
| D. | 蛋白质在紫外线、CuSO4溶液、福尔马林作用下均会发生变性 |
分析 A.葡萄糖分解生成乙醇和二氧化碳,葡萄糖不能水解;
B.检验葡萄糖,应在碱性溶液中;
C.煤制煤气,生成CO和氢气;
D.紫外线、CuSO4溶液、福尔马林均使蛋白质发生变性.
解答 解:A.葡萄糖分解生成乙醇和二氧化碳,葡萄糖不能水解,二糖、多糖可水解生成单糖,故A错误;
B.检验葡萄糖,应在碱性溶液中,则水解后,没有加碱至碱性,加入少量新制Cu(OH)2溶液,加热,不能检验,故B错误;
C.煤制煤气,生成CO和氢气,为化学变化,故C错误;
D.紫外线、CuSO4溶液、福尔马林均使蛋白质发生变性,为不可逆过程,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:实验题
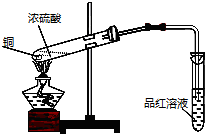
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11种 | B. | 13种 | C. | 14种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与电源正极相连的电极上发生还原反应 | |
| B. | 与电源负极相连的电极称为电解池的阴极 | |
| C. | 电解熔融氯化钠时,阳极上析出Cl2 | |
| D. | 电解是电能转化为化学能的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
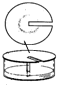 常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )
常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )| A. | 该方法为径向纸上层析法 | B. | 试样点需浸没于展开剂中 | ||
| C. | 试样点晾干或电风吹干后才能补滴 | D. | 喷浓氨水内层圆环色斑呈绛蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL | B. | 101mL | C. | 119mL | D. | 120mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+ Ba2+ A13+ |
| 阴离子 | OH- C1- SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com