
【题目】如图是1molCO(g)和2molH2(g)发生反应CO(g)+2H2(g)→CH3OH(g)过程中的能量变化曲线。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂时反应的能量变化。下列相关说法正确的是( )

A.使用催化剂后该反应从放热反应变成了吸热反应
B.使用和不使用催化剂相比反应的能量变化不同
C.1molCO(g)和2molH2(g)中的化学键完全被破坏需要吸收510kJ能量
D.1molCO(g)和2molH2(g)完全反应生成1molCH3OH(g)会释放出91kJ能量
科目:高中化学 来源: 题型:
【题目】FeS、FeS2在酸性条件下都能与重铬酸钾(K2Cr2O7)溶液反应,还原产物为Cr3+,氧化产物都是Fe3+、SO42-。等物质的量FeS、FeS2完全反应时,消耗氧化剂的物质的量之比为
A.5:3B.9:17C.3:5D.3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状 况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中,正确的是( )
A. 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B. 0.2 mol·L-1NH4Cl和0.1 mol·L-1NaOH溶液等体积混合后:c(![]() )>c(Cl-)>c(Na+)>c(OH-)>c(H+)
)>c(Cl-)>c(Na+)>c(OH-)>c(H+)
C. 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. 同浓度的下列溶液中,①(NH4)2SO4、②NH4Cl、③CH3COONH4、④NH3·H2O;c(![]() )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑,判断能否设计成原电池A._____________,B._____________。(填“能”或“不能”)
(2)将纯锌片和纯铜片图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是_______________。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲______________乙(填“>”、“<“或“=”)
③请写出图中构成原电池的负极电极反应式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)下列各组物质:
①金刚石和C60 ②H、D和T ③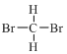 和
和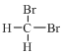 ④CH3(CH2)2CH3 和 (CH3)2CHCH3 ⑤正戊烷和异戊烷 ⑥(CH3)3CH2CH2CH3和CH3CH2CH2CH2CH3 ⑦H2O、T2O和D2O
④CH3(CH2)2CH3 和 (CH3)2CHCH3 ⑤正戊烷和异戊烷 ⑥(CH3)3CH2CH2CH3和CH3CH2CH2CH2CH3 ⑦H2O、T2O和D2O
互为同位素的是(填序号,下同)___,互为同素异形体的是______,互为同系物的是_____,属于同分异构体的是_______。
(2)书写下列物质的结构简式:
①2,6-二甲基-4-乙基辛烷:_________________
②2-甲基-1-戊烯:____________________
(3)按要求填空:
①分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简式: ______;
②C6H13Cl的同分异构体共有______种,请写出结构中仅含有四个甲基的所有同分异构体的结构简式:__________________。
③用系统命名法命名 ______________________________
______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。溶液变红的原因是_____。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。

①将下列实验操作步骤正确排序_____(填序号);重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.冷却至室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_____(列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中有气泡冒出,并可观察到C中出现白色沉淀、D中溶液褪色,则C、D中的溶液分别为_____、_____(填序号)。
a.浓H2SO4 b.NaOH c.BaCl2 d.Ba(NO3)2 e.品红
②写出硫酸亚铁高温分解反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在实验室浓盐酸和二氧化锰加热条件下可以反应生成氯化锰和Cl2等,某同学用此法制得标准状况下Cl2体积为22.4mL,据题意回答下列问题:
(1)写出其化学反应方程式并配平____________
(2)请计算共消耗MnO2多少克?_____________
(3)上述实验所用浓盐酸,其质量分数为36.5%,密度为1.19g/mL,为了使用方便,请计算该浓盐酸的物质的量浓度为多少?_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期VA族。D、E、H均为难溶于水的白色固体:化合物C、E均含A元素。其余物质均为中学化学中常见物质。
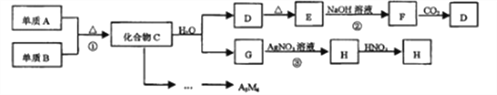
请回答:
(1)写出H的化学式:________________。
(2)化合物A3M4中含有的化学键类型为:________________。
(3)写出反应②的离子方程式:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com