
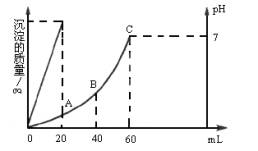
(1)最初混合液中硫酸和盐酸的物质的量浓度。
(2)在A点溶液的pH是多少?
(3)在B点溶液的pH是多少?
| 解:(1)从图示产生的沉淀量可知,当Ba(OH)2溶液加入20mL时,H2SO4被完全反应,设被Ba(OH)2中和H2SO4物质的量为x。
H2SO4+ Ba(OH)2 ══BaSO4↓+2H2O 1mol 1mol x 0.025mol×L-1´0.02L x=0.0005mol ∴ c( 加入60mLBa(OH)2时,溶液的pH等于7,说明,盐酸完全被中和,设HCl物质的量为y。 2HCl+ Ba(OH)2 ══BaCl2+2H2O 2mol 1mol y 0.025mol×L-1´(0.06-0.02)L y=2´10-3mol ∴ c(HCl)= (2)在A点时,由于已加入了20mL Ba(OH)2溶液,溶液的体积为(20+20)=40(mL),H2SO4已完全中和。HCl还未反应,溶液的c(H+)是由c(HCl)决定的。 ∴ c(H+)= (3)在B点加入的40mL Ba(OH)2溶液,其中20mL已和H2SO4反应,剩下的(40-20)mL Ba(OH)2溶液与盐酸反应。 2HCl + Ba(OH)2══BaCl2+2H2O 2mol 1mol 0.1mol×L-1´0.02L 0.025mol×L-1´ (0.04-0.02)L
剩余的HCl为:(0.1´0.02-2´0.025´0.02)mol=0.001mol
pH=-lg{(H+)}=-lg(1.7´10-
|


科目:高中化学 来源: 题型:
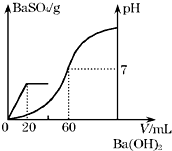 有H2SO4和HCl的混合溶液20mL,在溶液中加入0.025mol?L-1的Ba(OH)2溶液,生成的BaSO4的量和相对应的溶液的pH如图所示,求解下列问题:
有H2SO4和HCl的混合溶液20mL,在溶液中加入0.025mol?L-1的Ba(OH)2溶液,生成的BaSO4的量和相对应的溶液的pH如图所示,求解下列问题:查看答案和解析>>
科目:高中化学 来源:素质教育新教案 高中化学·二年级·第二册(上册) 题型:038
有H2SO4和盐酸的混合液20 mL,在溶液中加入0.025 mol/L的Ba(OH)2溶液时,生成BaSO4的量和溶液的pH值得到如下图所示的结果,求:
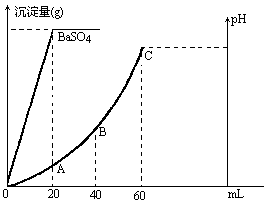
(1)最初混合液中硫酸和盐酸的物质的量浓度.
(2)在A点溶液的pH是多少?
(3)在B点溶液的pH是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:038
有H2SO4和盐酸的混合液20mL,在这溶液中加入0.025mol×L-1的Ba(OH)2溶液时,生成BaSO4的量和溶液的pH得到如图所示的结果,求:
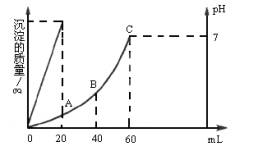
(1)最初混合液中硫酸和盐酸的物质的量浓度。
(2)在A点溶液的pH是多少?
(3)在B点溶液的pH是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:038
有H2SO4和HCl的混合溶液20 mL,在溶液中加入0.025 mol•L-1的Ba(OH)2溶液,生成的BaSO4的量和相对应的溶液的pH如图所示,求解下列问题(保留两冬天有效数字)。
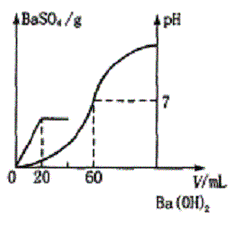
⑴最初混合溶液中H2SO4和盐酸的物质的量浓度;
⑵当加入Ba(OH)2体积分别为20 mL和40 mL时,溶液的pH各为多少?(lg5=0.69,lg6=0.78)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com