
温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率大于80%
CD
【解析】
试题分析:A.反应在前50 s的平均速率为v(PCl3)=(0.16mol÷2.0L)÷50 s=0.0016mol/(L·s);错误;B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol/L>0.20mol÷2.0L =0.10mol/L,说明升高温度,平衡正向移动,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,正反应方向是吸热反应,则反应的△H>0,错误;C.在相同温度下,若起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,则反应正向进行,在达到平衡前v(正)>v(逆),正确;D.在温度不变时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g)  PCl3(g)+Cl2(g)经一段时间后达到平衡的等效开始状态是1mol PCl3、1.0molCl2,由于平衡时PCl3的物质的量是0.2mol, PCl3的转化率是80%;而在相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,相当与给体系增大压强,增大压强,平衡向气体体积减小的逆反应方向移动,所以达到平衡时,PCl3的转化率大于80%,正确。
PCl3(g)+Cl2(g)经一段时间后达到平衡的等效开始状态是1mol PCl3、1.0molCl2,由于平衡时PCl3的物质的量是0.2mol, PCl3的转化率是80%;而在相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,相当与给体系增大压强,增大压强,平衡向气体体积减小的逆反应方向移动,所以达到平衡时,PCl3的转化率大于80%,正确。
考点:考查化学反应速率的计算、反应热的判断、反应进行的方向及物质的平衡含量的计算的知识。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2014秋江苏省东台市高二第一学期期中考试化学试卷(解析版) 题型:填空题
(19分)按要求填空:
(1)某有机物的结构简式为: ,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。
,该有机物中含氧官能团有: 、 、 、 (写官能团名称)。
(2)有机物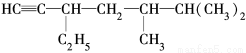 的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。
的系统名称是 ,将其在催化剂存在下完全氢化,所得烷烃的系统名称是 。
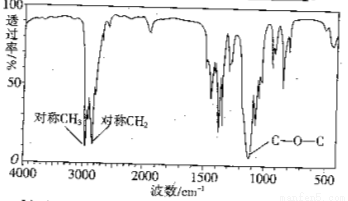
(3)下图是某一有机物的红外光谱图,该有机物的相对分子质量为74,则其结构简式为 。
(4)苯的同系物中,有的侧链能被酸性高锰酸钾溶液氧化,生成芳香酸,反应如下:
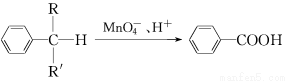
(R、R′表示烷基或氢原子)
①现有苯的同系物甲和乙,分子式都是C10H14。甲不能被酸性高锰酸钾溶液氧化为芳香酸,它的结构简式是 ;乙能被酸性高锰酸钾溶液氧化为分子式为C8H6O4的芳香酸,则乙可能的结构有 种。
②有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种。丙的结构简式共有四种,写出其余三种:
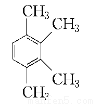 、 、 、 。
、 、 、 。
(5)已知:RCH=CHR,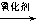 RCOOH+R,COOH。写出
RCOOH+R,COOH。写出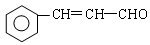 在强氧化剂条件下生成
在强氧化剂条件下生成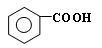 和另一种有机物 (写出其结构简式)。
和另一种有机物 (写出其结构简式)。
查看答案和解析>>
科目:高中化学 来源:2014秋广东省揭阳市高二第一学期期中考试化学试卷(解析版) 题型:实验题
(16分)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用如图所示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1的盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去。)
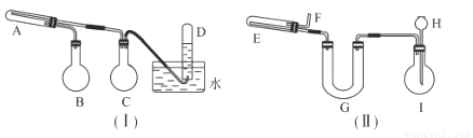
填写下列空白:
(1)实验进行时试管A中应加入的试剂是_________________;烧瓶B的作用是____________;烧瓶C的作用是_______________
(2)实验时,长颈漏斗H中应加入_____________________U型管G的作用是____________
(3)装置I中,在实验时需要加热的仪器是(填该仪器对应的字母)_________ ____ ;
当反应转移了4mol电子时,试管D中收集到的气体在标准状况下的体积为_____________。
(4)写出试管A中发生反应的化学方程式:________________________
查看答案和解析>>
科目:高中化学 来源:2014秋广东省揭阳市高二第一学期期中考试化学试卷(解析版) 题型:选择题
下列实验中,不能达到预期目的的是
A.向某未知溶液中滴加足量稀盐酸,再加几滴BaCl2溶液,检验SO42-的存在
B.用100mL量筒量取20.00mL Na2CO3溶液
C.不用另加任何试剂就能鉴别HCl 、Na2CO3 、Na2SO4 和BaCl2四种无色溶液
D.用粥汤检验淀粉溶液具有丁达尔效应
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(理)化学试卷(解析版) 题型:选择题
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4 B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③ D.N2的转化率:②>①>③
查看答案和解析>>
科目:高中化学 来源:2014秋广东省高二上学期期中考试(理)化学试卷(解析版) 题型:选择题
难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后加入适量碘并封管,置于加热炉中,发生反应:  。下列说法正确的是
。下列说法正确的是

A.在不同温度区域,TaI4 的量保持不变
B.在提纯过程中,I2 的量不断减少
C.该反应的平衡常数与TaI4 和S2 的浓度乘积成反比
D.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com