
碳、氮、氧是构成生命物质的三种主要元素。
(1)碳、氮、氧三种元素中,原子核外电子未成对电子数最多的是________(用元素符号表示)。
(2)已知CN-与N2结构相似,则HCN分子中 键与
键与 键数目之比为??????? 。
键数目之比为??????? 。
(3)H2O2分子中氧原子的杂化方式为___________。
(4)与NO2+互为等电子体的微粒有______、_______(举2例),NO3-的空间构型是_________。
(5)已知元素A的氧化物的晶胞结构如图所示,则该氧化物的化学式为_________。

(1)N (2)1:1 (3)sp3
(4)CO2、N2O、CNO-、SCN-等;平面三角形 (5)AO2
【解析】
试题分析:(1)根据核外电子排布规律可知,碳、氮、氧三种元素的核外电子排布分别为1s22s22p2、1s22s22p3、1s22s22p4,因此原子核外电子未成对电子数最多的是N元素。
(2)已知CN-与N2结构相似,因此含有三键,因此HCN分子的结构式为H-C≡N。由于单键都是 键,而三键是由1个
键,而三键是由1个 键与2个
键与2个 键构成的,所以HCN分子中
键构成的,所以HCN分子中 键与
键与 键数目之比为1:1。
键数目之比为1:1。
(3)H2O2分子中氧原子分别形成2个单键,另外还有2对孤对电子,所以氧原子的价层电子对数是4,因此氧原子的杂化方式为sp3。
(4)原子数和价电子数分别都相等的互为等电子体,组成NO2+微粒的有3个原子,价电子数是5+6×2-1=16,则与NO2+互为等电子体的微粒有CO2、N2O、CNO-、SCN-等;根据价层电子对互斥理论可知NO3-中含有的孤对电子对数= =0,因此价层电子对数是3,所以空间构型是平面三角形。
=0,因此价层电子对数是3,所以空间构型是平面三角形。
(5)已知元素A的氧化物的晶胞结构如图所示,则根据均摊法可知晶胞中A原子数=1+8× =2,O原子数=2+4×
=2,O原子数=2+4× =4,所以该氧化物的化学式为AO2。
=4,所以该氧化物的化学式为AO2。
考点:考查核外电子排布、共价键、杂化轨道类型、等电子体、分子空间构型以及晶胞结构与应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:


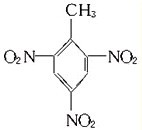





查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出由上述四种元素组成的可用作炸药的两种物质的结构简式。
①________________________②________________________
(2)写出由上述四种元素中的两种组成的天然高分子的结构简式(任写一种物质)。
(3)由上述四种元素中的三种组成的天然高分子化合物A,是人体所需要的三大营养物质之一。它在人体中某种酶的作用下发生________反应(填反应类型)。写出其反应生成的最终产物的化学方程式:________________________。
(4)B、C为两种共价化合物,它们均含上述四种元素,且互为同分异构体;它们的一个分子中都含有两个碳原子,B可以发生缩聚反应,C分子中含有40个电子。C的结构简式为________,B与NaOH溶液反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com