
科目:高中化学 来源: 题型:
下列说法正确的是
A.丙炔分子中三个碳原子位于同一直线上 B.丙烯与HCl加成只生成一种产物
C.1 mol丙烷在光照情况下,最多消耗4 mol氯气 D.丙烷中混有丙烯可用H2加热方法除去
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述正确的是
A.滴定管洗净后,直接注入标准液进行滴定
B.某溶液先加入稀盐酸无明显现象,再加入BaCl2溶液产生白色沉淀,说明原溶液中含有SO42-
C.配制一定物质的量浓度的稀硫酸时,向容量瓶中加入适量的水,再缓缓注入事先量取的浓硫酸
D.某气体能使湿润的蓝色石蕊试纸变为红色,则该气体为氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是
A.氯化铝溶液中加入过量氨水反应实质是:
B.在加入铝粉能放出氢气的溶液中: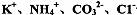 一定能够大量共存
一定能够大量共存
C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液
D.依据铝热反应原理,能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
锂碘电池可用于心脏起搏器的电源。该电池反应为:
已知:

下列结论中,不正确的是
A.电池反应2Li(s)+I2(s)=2LiI(s) △H= -105 kJ·mol-1
B.电池正极反应Li-e—=Li+
C.当有14 gLi消耗时,理论上会释放2mol e—的电量
D.该电池放电完毕电池的总质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+C+S KCl+CO2 ↑+SO2↑,下列判断不正确的是
KCl+CO2 ↑+SO2↑,下列判断不正确的是
A.若反应中C和S的质量比为3:4,则n(KClO3):n(CO2)为1:1
B.若反应中C和S的质量比为3:16,则n(KClO3):n(CO2)为2:1
C.SO2通人NaHCO3溶液产生CO2,可证明非金属性S强于C
D.KClO3与SO2在强酸性溶液中反应制得ClO2,可证明SO2的还原性强于ClO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,离子浓度的关系一定正确的是
A.氨水中逐滴加入盐酸得到酸性溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.pH相同的CH3COONa溶液、Ba(OH)2溶液、KHCO3溶液:c(K+)>c(Na+)>c(Ba2+)
C.物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合:
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
D.将等物质的量的KHC2O4和H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-)+c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为
(2)工业上生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
 |
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
步骤一应调节溶液的pH范围是 ,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因
 ②步骤三中的具体操作方法是
②步骤三中的具体操作方法是
(3)有人提出可以利用如图的装置从溶液B中提炼金属铜。该过程中右边电极的反应式是 ,若装入B溶液500mL(电解前后溶液体积变化可忽略),当阴极增重1.6g时,停止通电,则反应后溶液的pH= 。
(4)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) ΔH
已知:①2Cu(s)+1/2O2(g)=Cu2O(s) ΔH=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s) ΔH=-79.5kJ/mol
③S(s)+O2(g)=SO2(g) ΔH=-296.8kJ/mol
则该法冶炼铜的反应中ΔH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式: 。
(2)装置B中饱和食盐水的作用是 ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象: 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是 (填字母编号)。
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 ,该现象 (填“能”或“不能”)说明溴单质的氧化性强于碘,原因是 。
(5)装置F的作用是 ,其烧杯中的溶液不能选用下列中的 (填字母编号)。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com