
| A. | Al3+的结构示意图: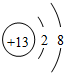 | B. | NaClO的电子式: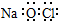 | ||
| C. | 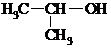 的名称:2-甲基乙醇 的名称:2-甲基乙醇 | D. | 乙醛分子的比例模型: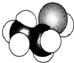 |
分析 A.铝离子的核电荷数为13,核外电子总数为10,最外层达到8电子稳定结构;
B.次氯酸钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
C.该有机物主链为丙醇,羟基在2号C;
D. 表示的有机物的结构简式为CH3CH2OH,为乙醇,不是乙醛.
表示的有机物的结构简式为CH3CH2OH,为乙醇,不是乙醛.
解答 解:A.铝离子的核电荷数为10,最外层为8个电子,Al3+的结构示意图为: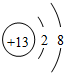 ,故A正确;
,故A正确;
B.次氯酸钠由钠离子和次氯酸根离子构成,其正确的电子式为: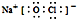 ,故B错误;
,故B错误;
C.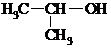
D. 表示的为CH3CH2OH,而乙醛的结构简式为CH3CHO,乙醛的比例模型为:
表示的为CH3CH2OH,而乙醛的结构简式为CH3CHO,乙醛的比例模型为: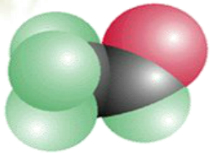 ,故D错误;
,故D错误;
故选A.
点评 本题考查了常见化学用语的判断,题目难度中等,涉及电子式、离子结构示意图、比例模型、有机物的命名等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生规范答题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| B. | 为除去溴苯中的溴,可用NaOH溶液洗涤,再分液 | |
| C. | 为除去乙炔气中少量的H2S,可使其通过CuSO4 溶液 | |
| D. | 为除去CO2 中少量的SO2 ,可使其通过饱和Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 稳定性 | 得电子能力 | 离子半径 | 电负性 |
| CH4<NH3 | 1H=2H | Na+>Al3+ | C>Al |
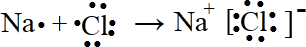 .
.| 化学键 | H-H | H-Cl | Cl-Cl |
| 键能kJ/mol | a | b | c |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
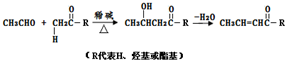
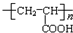 +HOCH2CH2OH$→_{△}^{浓硫酸}$
+HOCH2CH2OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O. +NaOH→
+NaOH→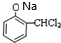 +H2O.
+H2O. .
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某研究性小组将一定浓度的NaCO3溶液滴入MgSO4溶液中得到白色沉淀,对于白色沉淀的成分进行研究:
某研究性小组将一定浓度的NaCO3溶液滴入MgSO4溶液中得到白色沉淀,对于白色沉淀的成分进行研究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
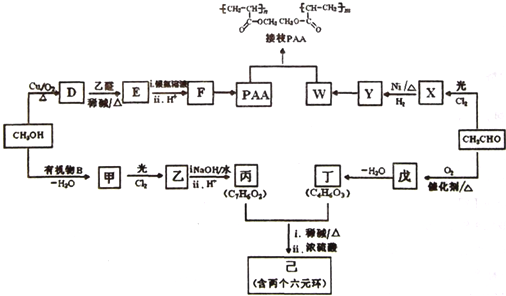
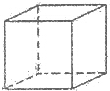 己知A、B、C、D、E、F、G、H八种元素都是周期表中前四周期的元素,它们的核电荷数依次增大,A是原子半径最小的主族元素,B有三种不同的能级且每种能级上所含电子数相同,C的单质性质稳定且一种氢化物极易溶于水,D能形成两种互为同素异形体的气态单质,A、D、E的核内质子数之和与F的核内质子数相同,F的基态原子中有4个未成对电子,G比F原子多一个核内质子,上述H元素的+l价阳离子的K、L、M能层为全充满结构.
己知A、B、C、D、E、F、G、H八种元素都是周期表中前四周期的元素,它们的核电荷数依次增大,A是原子半径最小的主族元素,B有三种不同的能级且每种能级上所含电子数相同,C的单质性质稳定且一种氢化物极易溶于水,D能形成两种互为同素异形体的气态单质,A、D、E的核内质子数之和与F的核内质子数相同,F的基态原子中有4个未成对电子,G比F原子多一个核内质子,上述H元素的+l价阳离子的K、L、M能层为全充满结构.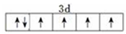 .在这两种离子之间Fe3+更稳定(填化学式):从微观结构角度解释该离子更稳定的原因:Fe3+离子的3d轨道为半满稳定状态.
.在这两种离子之间Fe3+更稳定(填化学式):从微观结构角度解释该离子更稳定的原因:Fe3+离子的3d轨道为半满稳定状态.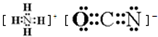
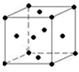 .该晶体中H原子直径为apm,H的相对原子质量为M,阿伏伽德罗常数为NA,求该晶胞密度表达式$\frac{\sqrt{2}M×1{0}^{30}}{{N}_{A}{a}^{3}}$g/cm3(用a,M,NA表示)
.该晶体中H原子直径为apm,H的相对原子质量为M,阿伏伽德罗常数为NA,求该晶胞密度表达式$\frac{\sqrt{2}M×1{0}^{30}}{{N}_{A}{a}^{3}}$g/cm3(用a,M,NA表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1 mol•L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(OH-) | |
| B. | 若将0.1mol•L-1BOH溶液稀释至0.001 mol•L-1则溶液的pH=10 | |
| C. | 若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+) | |
| D. | 若将上述两溶液按体积比l:2混合,则混合液中:c(B+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com