
【题目】下列关于卤素(F、Cl、Br、I)叙述正确的是( )
A.其单质在常压下的沸点,随着卤素核电荷数的增多逐渐降低
B.单质和水反应通式:X2+H2O=HX+HXO(用X表示卤素),剧烈程度随着核电荷数的增多而减弱
C.单质和氢气反应的通式:X2+H2=2HX(条件不同),剧烈程度随着卤素核电荷数的增多而减弱
D.随着卤素核电荷数的增多,单质的氧化性逐渐增强
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】对H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学们分别设计了如图甲、乙所示的实验装置。请回答相关问题:

(1)定性如图甲可通过观察_________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______。
(2)定量用图乙所示装置做对照试验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在工业生产、生命科技等行业有重要应用。
(1)Co的价电子排布式为__,的I4(Co)__的I4(Fe)(填>、<或者=),原因是__。
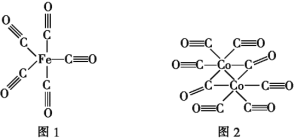
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8的结构如图1、图2所示,图1中0.1molFe(CO)5含有配位键__个,写出2个与CO互为等电子体微粒__,图2中的σ键和π键个数之比是__(填元素符号)。
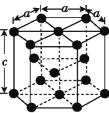
(3)金属钴的堆积方式为六方最密堆积,其配位数是__;该晶胞的边长为xnm,高为ynm,该晶胞的密度为__g·cm-3。(NA表示阿伏加德罗常数的值,列出代数式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置及药品能实现相应实验目的的是
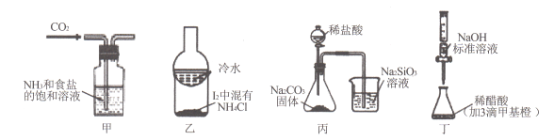
A. 甲用于制取NaHCO3晶体 B. 乙用于分离I2和NH4Cl
C. 丙用于证明非金属性强弱:Cl>C>Si D. 丁用于测定某稀醋酸的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:
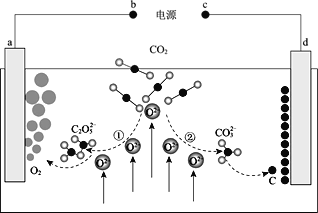
下列说法不正确的是( )
A.b为电源的正极
B.①②中,捕获 CO2 时碳元素的化合价发生了变化
C.a 极的电极反应式为:![]()
D.上述装置存在反应:CO2=C + O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可提取各种化工产品,下图是工业上对海水的一种综合利用的流程图:
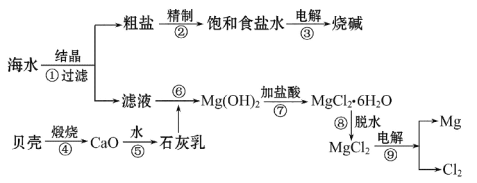
(1)上述流程图①~⑨步骤中,属于氧化还原反应的是__________(填序号);
(2)若粗盐中仅含有Ca2+、Mg2+两种杂质离子。精制提纯时,备用的除杂试剂有:(A.盐酸、B.Na2CO3溶液、C.NaOH溶液)。请你正确排列加入的顺序:__________(填编号);
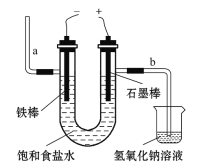
(3)用如图电解饱和食盐水,石墨棒上产生的气体为Cl2;在铁棒周围的溶液里滴加紫色石蕊试液,溶液变成_____________色;
(4)在盛有Mg(OH)2固体的烧杯中,加入足量盐酸,待固体全部溶解后,要从溶液中获取MgCl2·6H2O晶体,需要进行的实验操作依次为__________(填编号)。
A.蒸馏 B.蒸发 C.冷却结晶 D.晶体灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛分子结构式如图,用2个Cl取代甲醛中的H可得到碳酰氯,下列描述正确的是( )
![]()
A.甲醛分子和碳酰氯分子是等电子体
B.碳酰氯分子中的C原子为手性碳原子
C.甲醛分子中的H-C-H键角与碳酰氯分子中的Cl-C-Cl相等
D.碳酰氯分子为平面三角形,分子中存在有3个σ键、1个π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com