
| A.非极性共价键 | B.极性共价键 | C.配位键 | D.离子键 E.氢键 |
 平面三角形 (2)F>N>O F>N>C(3)HCl(4)BCD
平面三角形 (2)F>N>O F>N>C(3)HCl(4)BCD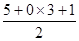 =3,N周围有3对电子对,无孤对电子,NO3-为平面三角形。
=3,N周围有3对电子对,无孤对电子,NO3-为平面三角形。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:不详 题型:推断题
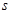 键与π键的键数之比为 。
键与π键的键数之比为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
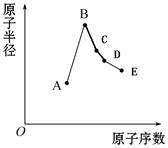
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Z<Y<W,而离子半径:W<Y<Z |
| B.W的氯化物水溶液中滴加过量Z与钠形成的饱和溶液,可生成W配合物 |
| C.由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度大于酸根离子浓度 |
| D.已知YX3沸点远高于YZ3,则Y—X键的键能高于Y—Z键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.共价化合物中只含共价键,离子化合物中只含离子键 |
| B.第三周期元素形成的氢化物稳定性从左到右逐渐增强 |
| C.短周期元素形成简单离子后,最外层电子数均达到8(或2)稳定结构 |
| D.在周期表过渡元素中寻找半导体材料,在金属与非金属分界处寻找催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
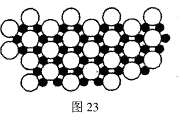
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com