
【题目】.在一定温度和压强下,2体积X2(g)跟3体积Y2(g)化合生成2体积化合物M(g),则化合物M的化学式是( )
A.XY3B.X2Y3C.X3YD.XY
科目:高中化学 来源: 题型:
【题目】有机物F(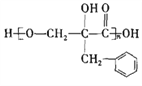 )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:
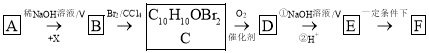
已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②
请回答下列问题:
(1)X的化学名称是__________。
(2)B生成C的反应类型为__________。
(3)E的结构简式为__________。
(4)由C生成D的化学方程式为____________________________________________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和![]() 溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为6:2:2:1:1.写出两种符合要求的Y的结构简式:__________、__________。
溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为6:2:2:1:1.写出两种符合要求的Y的结构简式:__________、__________。
(6)写出以乙醛和乙二醇为主要原料合成高分子化合物(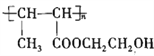 )的合成路线(无机试剂自选):__________________________________________________。
)的合成路线(无机试剂自选):__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,三种难溶银盐的Ksp与颜色如右表,下列说法正确的是
AgCl | Ag2CrO4 | AgI | |
颜色 | 白 | 砖红 | 黄 |
Ksp | 1.8×10-10 | 1.0×10-12 | 8.5×10-17 |
A.AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减小
B.Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6mol·L-1
C.向AgCl悬浊液加入足量KI溶液,沉淀将由白色转化为黄色
D.向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和1mol B气体在2 L的容器内混合,在一定条件下发生反应: 2A(g) +B(g)![]() 3C(g),若2 min后测得C的浓度为0.6 mol·L-1,则下列说法正确的是
3C(g),若2 min后测得C的浓度为0.6 mol·L-1,则下列说法正确的是
A. 用物质A表示反应的平均速率为v(A)= 0.4 mol·(L·min)-1
B. 2 min时A、B、C三种气体的总量为5mol
C. 2 min时B的转化率为20%
D. 若2 min后该反应达平衡,则各种气体的量不再变化,反应停止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g) △H<0一定条件下在某密闭容器中达到平衡。t1时改变某一条件,反应速率与时间关系如下图。下列说法中正确的是( )
2SO3(g) △H<0一定条件下在某密闭容器中达到平衡。t1时改变某一条件,反应速率与时间关系如下图。下列说法中正确的是( )
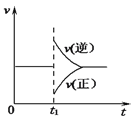
A. 维持温度、反应体系体积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度不变,t1时扩大反应体系体积
D. 维持温度、容器体积不变,t1时充入SO3(g),同时减少SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g) + B(g) ![]() xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
xC(g) + 2D(g)。2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol·L-1。下列判断错误的是
A. x=1
B. B的转化率为50%
C. 2min内A的反应速率为0.3mol·L-1·min-1
D. 若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“小于”或“等于”)醋酸的电离平衡常数,理由是__________________。
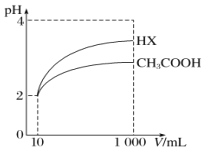
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对废弃物的回收处理可以从源头上减少环境污染,不符合该理念的是
A. 废旧书刊焚烧处理 B. 废旧铅蓄电池回收金属铅
C. 将垃圾分类并回收处理 D. 废旧汽车回收钢铁和塑料等材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,用 Fe2O3、 NiO 或 Cr2O3作催化剂对燃煤烟气进行回收,使 SO2转化生成为 S。催化剂不同,相同其他条件(浓度、温度、压强)情况下, 相同时间内 SO2 的转化率随反应温度的变化如下图:下列说法不正确的是( )
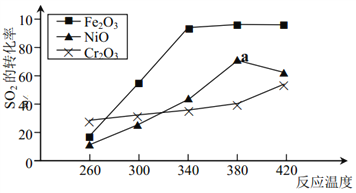
A. 不考虑催化剂价格因素,选择 Fe2O3 作催化剂可以节约能源
B. 相同其他条件下,选择 Cr2O3 作催化剂, SO2 的平衡转化率最小
C. a 点后 SO2 的转化率减小的原因可能是温度升高催化剂活性降低了
D. 选择 Fe2O3 作催化剂,最适宜温度为 340~380℃温度范围
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com