
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+ ![]() O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
【答案】C
【解析】A、燃烧热是指1mol可燃物燃烧释放的热量,1molCO燃烧放热283kJ,故A错误;B、根据2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=+452kJ·mol-1可知,Na2O2(s)+CO2(s) =Na2CO3(s)+ ![]() O2(g) △H=+226kJ·mol-l,故B错误;C、已知:①2CO(g)+O2(g)═2CO2(g) △H=-566kJ/mol,②Na2O2(s)+CO2(g)═Na2CO3(s)+
O2(g) △H=+226kJ·mol-l,故B错误;C、已知:①2CO(g)+O2(g)═2CO2(g) △H=-566kJ/mol,②Na2O2(s)+CO2(g)═Na2CO3(s)+ ![]() O2(g)△H=-226kJ/mol,据盖斯定律(①+②×2)÷2得:CO(g)+Na2O2(s)=Na2CO3(s) △H=509kJ/mol,反应中C由+2价变成+4价,电子转移数为2mol,故C正确;D、燃烧热是指1mol可燃物燃烧释放的热量,根据2CO(g)+O2(g) =2CO2(g) △H=-566kJ·mol-1,CO的燃烧热为283kJ·mol-1,故D错误;故选C。
O2(g)△H=-226kJ/mol,据盖斯定律(①+②×2)÷2得:CO(g)+Na2O2(s)=Na2CO3(s) △H=509kJ/mol,反应中C由+2价变成+4价,电子转移数为2mol,故C正确;D、燃烧热是指1mol可燃物燃烧释放的热量,根据2CO(g)+O2(g) =2CO2(g) △H=-566kJ·mol-1,CO的燃烧热为283kJ·mol-1,故D错误;故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式__________(中和热数值为57.3kJ/mol)。
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因不可能是_______(填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是__________________________。
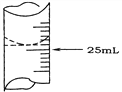
(2)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图,则此时消耗标准溶液的体积为___________。
乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.11 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.22 | 26.31 |
(3)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为________________(小数点后保留四位)。
(4)下列哪些操作会使测定结果偏高___________(填序号)。
A.锥形瓶用蒸馏水洗净后,直接注入待测溶液进行滴定
B.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
C.碱式滴定管用蒸馏水洗涤后立即取用25.00mL待测液注入锥形瓶中进行滴定
D.滴定前俯视滴定管读数,滴定后平视滴定管读数
(5)滴定达到终点的标志是_________________________________________________。
【答案】 H+(aq)+OH-(aq)= H2O(l)△H=-57.3kJ·mol-1 B 用碱液润洗 23.80mL 0.1044 mol·L-1 BD 滴入最后一滴标准液,溶液由红色变为无色,且半分钟内不复原
【解析】 I.(1).强酸强碱的中和热为-57.3kJ/mol,即强酸和强碱的稀溶液完全反应生成1mol水放出的热量为57.3kJ,则稀盐酸和稀氢氧化钠溶液反应的中和热的热化学方程式:H+(aq)+OH-(aq)= H2O(l) △H=-57.3kJ·mol-1;故答案为:H+(aq)+OH-(aq)= H2O(l) △H=-57.3kJ·mol-1;
(2).A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度,则残留在温度计上的NaOH会与盐酸反应,使盐酸的起始温度偏高,温度差偏小,中和热的数值偏小,故A正确;B.量取盐酸的体积时仰视读数,会导致所量取的盐酸体积偏大,放出的热量偏高,中和热的数值偏大,故B错误;C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中,热量散失较多,中和热的数值偏小,故C正确;D.装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故D正确;因此答案选B
II. (1)碱式滴定管用蒸馏水洗净后,接下来应该用待测的NaOH溶液进行润洗,否则会将NaOH溶液稀释,造成实验误差,故答案为:用碱液润洗;
(2).由图可知,滴定后液面的读数为:24.90mL,因滴定前滴定管内液面读数为1.10 mL,则此时消耗标准溶液的体积为:(24.90-1.10)mL=23.80mL,故答案为:23.80mL;
(3).由表中数据可知,第1次消耗标准液的体积是:(26.11-0.00)mL=26.11mL,第2次消耗标准液的体积是:(33.30-1.56)mL=31.74mL,第3次消耗标准液的体积是:(26.31-0.22)mL=26.09mL,因第2次数据误差较大,故舍去,则消耗标准液的平均体积是:(26.11+26.09)mL÷2=26.10mL,所以NaOH溶液的物质的量浓度为:c(NaOH)=![]() = 0.1044 mol·L-1,故答案为:0.1044 mol·L-1;
= 0.1044 mol·L-1,故答案为:0.1044 mol·L-1;
(4). A.锥形瓶用蒸馏水洗净后,直接注入待测溶液进行滴定,对实验结果无影响,故A错误;B.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液,则消耗标准液体积偏大,测定结果偏高,故B正确;C.碱式滴定管用蒸馏水洗涤后立即取用25.00mL待测液注入锥形瓶中进行滴定,则所取待测液偏少,消耗标准液的体积偏少,测定结果偏低,故C错误;D.滴定前俯视滴定管读数,滴定后平视滴定管读数,则导致所量取的标准液体积偏大,测定结果偏高,故D正确;答案选BD;
(5). 到滴定终点时,当滴入最后一滴标准液,溶液会由红色变为无色,且半分钟内不复原,故答案为:滴入最后一滴标准液,溶液由红色变为无色,且半分钟内不复原。
【题型】实验题
【结束】
26
【题目】铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
温度/℃ | 1 000 | 1 150 | 1 300 |
平衡常数 | 64.0 | 50.7 | 42.9 |
请回答下列问题:
①该反应的平衡常数表达式K=__________,ΔH_______0(填“>”、“<”或“=”)。
②欲提高反应中CO的平衡转化率,可采取的措施是_____________________。
A.减少Fe的量 B.加入合适的催化剂
C.增大容器的体积 D.降低反应的温度
③在一个容积为1 L的密闭容器中,1000 ℃时加入Fe2O3、CO各2 mol,反应经过10 min后达到平衡。求该时间范围内反应的平均反应速率v(CO)=______________,Fe2O3的平衡转化率为________。
(2)饱和Mg(OH)2溶液中滴加FeCl3溶液,产生红褐色沉淀, 反应的离子方程式是________________________________________。
(3)已知:2Fe(s)+3/2O2(g)=Fe2O3(s) △H=824 kJ·mol-1、2Al(s)+3/2O2(g)=Al2O3(s) △H=1675.7 kJ·mol-1。则铝与Fe2O3发生反应生成Al2O3和Fe的热化学方程式为 :___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.甲烷中混有少量乙烯可用酸性高锰酸钾溶液除去
B.苯和乙烯都有碳碳双键所以都能使溴水褪色
C.相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同
D.在一定条件下,苯与氯气生成氯苯的反应类型是加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g)![]() 2NH3(g) H=-92.2 kJ·mol-1 ,据此回答以下问题:
2NH3(g) H=-92.2 kJ·mol-1 ,据此回答以下问题:
(1)①某温度下,若把 10 mol N2 与 30 mol H2置于体积为 10 L 的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为 20%,则该温度下反应的K=_______ (可用分数表示)。
②对于合成氨反应而言,下列有关图像一定正确的是______(选填序号)。
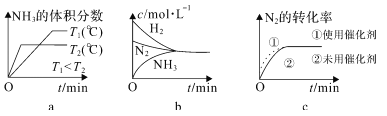
③在碱性溶液中通过电解法可以实现由 N2 制取 NH3:2N2+6H2O![]() 4NH3+3O2,阴极的电极反应式是_______________。
4NH3+3O2,阴极的电极反应式是_______________。
(2)室温下,若将 0.1 mol·L-1 盐酸滴入 20 mL 0.1 mol·L-1 氨水中,溶液 pH 随加入盐酸体积的变化曲线如下图所示。
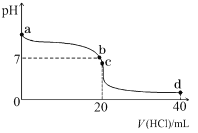
①NH3·H2O 的电离方程式是_______________。
②b 点所示溶液中的溶质是_______________。
③c 点所示溶液中,离子浓度从大到小的关系为_______________。
④常温下,若将 amol/LNH3·H2O 与等体积的 bmol/L 的盐酸混合,充分反应后溶液呈中性(不考虑氨水和盐酸的挥发),则该温度下 NH3·H2O 的电离常数Ka=___________(用含 a 和 b 的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏伽德罗常数)( )
A. 58.5g NaCl含有σ键的个数为2NA
B. 12 g石墨中含有C--C键的个数为3NA
C. 12 g金刚石中含有C--C键的个数为2NA
D. 78 g苯中含有C==C键的个数3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃ 时,1LpH=1的H2SO4溶液中含有0.1NAH+
B. 常温常压下,18gD2O含有的质子数为10NA
C. 9.0g淀粉和葡萄糖的混合物中共含有0.3NA碳原子
D. 铜粉与硫粉混合加热,每消耗1mol铜粉,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2 mol·L-1·min -1,2min 末 N2 的浓度为7 mol·L-1,则氢气的起始浓度为
A.9 mol·L-1
B.6 mol·L-1
C.3 mol·L-1
D.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变a1mol/L元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示,已知[δ(X)= ![]() ]。
]。
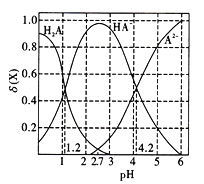
下列叙述错误的是
A. lg[K2(H2A)]=-4.2;pH=2.7时,c(HA-)>c(H2A)=c(A2-)
B. pH=4.2时,c(HA-)=c(A2-)>c(H+);随着pH的升高,c(HA-)/c(H2A)的比值先增大后减小
C. 0.1mol/L的NaHA溶液中存在:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol/L
D. pH=1.2时,c(H2A)=c(HA-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com