
【题目】如图所示,在常温下,将铁棒和石墨棒插入盛有足量饱和NaCl溶液的U型管中,下列分析正确的是( )
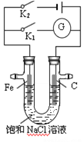
A. K1闭合,Na+向铁棒移动
B. K1闭合,碳棒上发生的反应为2H++2e—=H2↑
C. K2闭合,电路中通过0.2NA个电子时,石墨电极上生成2.24L标况下气体
D. K2闭合,铁棒不易被腐蚀,电路中通过0.001NA个电子时,摇匀后溶液的pH为11
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】NOx是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去NOx的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。
请完成下列问题:
(1)汽车发动机工作时会引发反应N2(g)+O2(g)![]() 2NO(g)。2000 K 时,向固定容积的密闭容器中充入等物质的量的N2、O2 发生上述反应,各组分体积分数(φ)的变化如图1所示。N2 的平衡转化率为_____________。
2NO(g)。2000 K 时,向固定容积的密闭容器中充入等物质的量的N2、O2 发生上述反应,各组分体积分数(φ)的变化如图1所示。N2 的平衡转化率为_____________。

(2)在密闭、固定容积的容器中,一定量NO发生分解的过程中,NO 的转化率随时间变化关系如图2 所示。
①反应2NO(g)![]() N2(g)+O2(g) △H_______0 (填“>”或“<” )。
N2(g)+O2(g) △H_______0 (填“>”或“<” )。
②一定温度下,能够说明反应2NO(g)![]() N2(g)+O2(g)已达到化学平衡的________(填序号)。a.容器内的压强不发生变化 b.混合气体的密度不发生变化
N2(g)+O2(g)已达到化学平衡的________(填序号)。a.容器内的压强不发生变化 b.混合气体的密度不发生变化
C.NO、N2、O2 的浓度保持不变 d.2v(NO)正=v(N2 )逆
(3)干法脱硝:SCR(选择性催化剂法)技术可有效降低柴油发动机在空气过量条件下的NO 排放。其工作原理如下:

①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为____________。
②反应器中NH3 还原NO 的化学方程式为____________________。
(4)湿法脱硝:采用NaClO2 溶液作为吸收剂可对烟气进行脱硝。323 K 下,向足量碱性NaClO2 溶液中通入含NO 的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
离子 | NO3- | NO2- | Cl- |
c/(mol L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
①NaClO2 溶液显碱性,用离子方程式解释原因_______________________。
②依据表中数据,写出NaClO2溶液脱硝过程中发生总反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是(N﹣14 O﹣16 C﹣12 H﹣1)( )
A.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA
B.标准状况下,22.4 L CH2Cl2中含有的氯原子数目为2NA
C.16g CH4与18 g NH4+ 所含质子数相等
D.1molCu在足量硫蒸气中反应时转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块生物组织或结构捣碎后进行化学分析,得知其中含有水、蛋白质、DNA和糖原等成分,由此可判断该组织或结构是 ( )
A.SARS病毒 B.家兔的肝脏 C.甜菜的块根 D.细菌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示进行实验,下列说法不正确的是
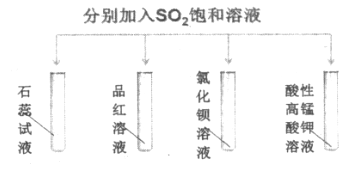
A. 石蕊试液变红说明SO2的水溶液显酸性
B. 品红溶液、酸性高锰酸钾溶液褪色原因不相同
C. BaCl2溶液中开始没有明显现象,一段时间后缓慢出现浑浊,该浑浊为BaSO3
D. 该实验说明SO2的性质具有多样性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法不正确的是
A. 甲、乙、丙三种物质都含有氮元素 B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用 D. 丁为NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸的流程如下图所示。己知黄铁矿的主要成分是FeS2(二硫化亚铁)。

请回答下列问题:
(1)FeS2中铁元素的化合价是_____________。
(2)接触室中生成SO3的化学方程式是_____________________。
(3)从接触室中出来并被循环利用的物质是______________________。
(4)工业上采用氨水处理尾气中的SO2,请写出足量氨水和SO2反应的离子方程式____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年中国首次海域可燃冰(CH4·nH2O,密度ρ1 g·cm-3)试开采成功。若以辛烷代表汽油(密度ρ2 g·cm-3)的组成,下列说法不正确的是
① CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH1 = —a kJ·mol-1
② 2C8H18(l) + 25O2(g) =16CO2 (g) + 18H2O(l) ΔH 2 = —b kJ·mol-1
A. 可燃冰适宜保存在低温,高压的环境中
B. 1 m3可燃冰可释放出标准状况下![]() m3的CH4
m3的CH4
C. 汽油的燃烧热约为0.5b kJ·mol-1
D. 1m3可燃冰释放出的甲烷燃烧放出的热量约为等体积汽油的![]() 倍
倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图表示正确的是

A. A图表示Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H1=+26.7kJ/mol反应的能量变化
B. B图表示碳的燃烧热
C. C图表示实验的环境温度20℃,将物质的量浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)
D. D图己知稳定性顺序:B![]() B
B![]() C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)
C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com