
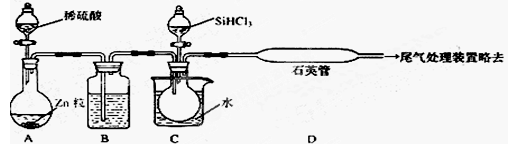


科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
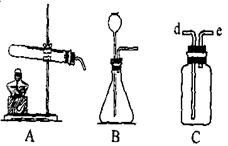
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。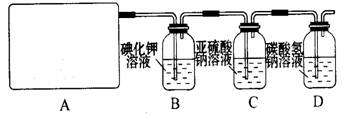
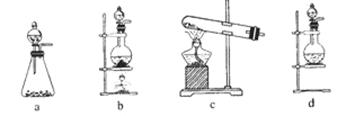
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
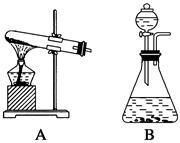
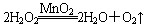 。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。
。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②⑥③⑦⑤ | B.④③⑤⑦⑥ | C.①③⑦⑤⑥ | D.②⑤⑦⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 |
| B.乙烷中混有乙烯,通H2在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓H2SO4和浓HNO3,将其倒入NaOH溶液中,静置,分液 |
| D.乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.先热过滤,后常温减压过滤 | B.先常温常压过滤,后常温减压过滤 |
| C.先常温减压过滤,后热过滤 | D.两次都用减压过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
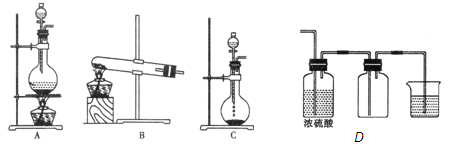
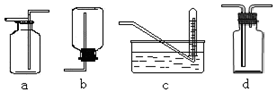
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com