
| A. | FeCl3与Na2S | B. | Ca(HCO3)2与Ca(OH)2 | C. | HCl与NaHCO3 | D. | AgNO3与NH3•H2O |
分析 与反应物的量无关时,只发生一个化学反应,则就能用同一离子方程式表示,以此来解答.
解答 解:A.无论量的多少都只发生FeCl3与Na2S的氧化还原反应生成硫化亚铁、S、NaCl,则能用同一离子方程式表示,故A不选;
B.无论量多少,均发生Ca(HCO3)2+Ca(OH)2═2CaCO3↓+2H2O,能用同一离子反应方程式表示,故B不选;
C.无论量多少,均防晒霜的HCl+NaHCO3═NaCl+CO2↑+H2O,能用同一离子方程式表示,故C不选;
D.一水合氨少量,生成AgOH,一水合氨过量生成银氨溶液,不能用同一离子方程式表示,故D选;
故选D.
点评 本题考查与量有关的离子反应的书写,为高频考点,明确量对化学反应的影响是解答本题的关键,注意与量有关的离子反应及氧化还原反应的分析,题目难度较大.


科目:高中化学 来源: 题型:解答题
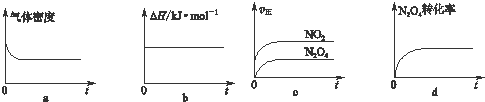
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
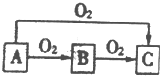 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )| A. | 等浓度的两种酸其酸性相同 | |
| B. | 两种酸都能与溴水发生加成反应 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 鞣酸能与Fe3+发生显色反应,而莽草酸不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
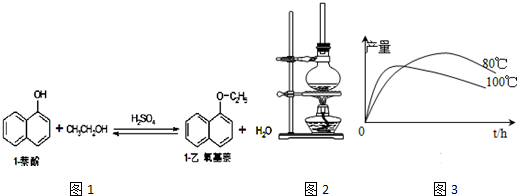
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
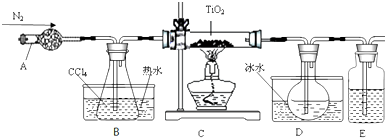
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳只存在金刚石和石墨两种同素异形体 | |
| B. | Mg、MgO中微粒的半径:r(O2-)>r(Mg2+)>r(Mg) | |
| C. | 在该反应条件下,Mg的还原性强于C的还原性 | |
| D. | 相同质量的镁在足量的CO2和O2中完全燃烧,固体质量增重相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com