
【题目】下列我国合成的材料中,主要成分由同周期两种元素组成的是
A.可实现高温超导的钙钛矿(CaTiO3)薄膜
B.制造大口径高精度非球面反射镜的碳化硅材料
C.大面积单品六方氮化硼半导体材料
D.可淡化海水的石墨烯纳米网
科目:高中化学 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示:
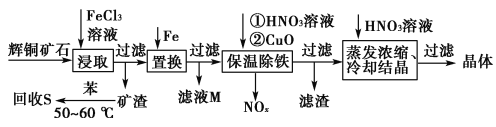
(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:______________________________________________________________。
(2)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是______________________________________________________________。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为_________________________________________________;
向滤液M中加入(或通入)________(填字母),可得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
(4)“保温除铁”过程中,加入CuO的目的是__________;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是:
A.升高温度,可提高活化分子百分数,使有效碰撞几率提高,化学反应速率加快
B.碱性溶液均可以使无色酚酞试液变红色
C.pH=7的溶液中,Na+、Al3+、Cl-、NO3-可以大量共存
D.同类物质,键能越大,稳定性越弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组物质中含有的化学键类型相同的是( )
A. NaCl、HCl、H2O、NaOH B. HBr、CO2、H2O、CS2
C. Cl2、Na2S、HCl、SO2 D. Na2O2、H2O2、H2O、O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
① CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H=______kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H=______kJ·mol-1。
(2)反应①达平衡后采取下列措施,能提高CH3OH产率的有__________。
A.加入H2 B.升高温度 C.增大压强 D.使用催化剂
(3)在一定温度下,将4mol CO和4mol H2混合置于2L的密闭容器中发生反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),60s时达到平衡状态时,测得气体的总物质的量为4mol。达平衡时,氢气的转化率为__________,用CO表示的反应速率为__________,该反应的平衡常数为__________。
CH3OCH3(g)+CO2(g),60s时达到平衡状态时,测得气体的总物质的量为4mol。达平衡时,氢气的转化率为__________,用CO表示的反应速率为__________,该反应的平衡常数为__________。
(4)以下说法能说明反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)达到平衡状态的有__________。
CH3OCH3(g)+CO2(g)达到平衡状态的有__________。
A. 氢气和二氧化碳的浓度之比为3∶1
B.单位时间内断裂3个H-H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(5)二甲醚燃料电池的工作原理如图所示:
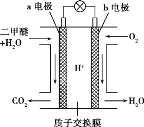
该电池负极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的说法不正确的是 ( )
A. 化石能源物质内部贮存着大量的能量
B. 植物的光合作用使太阳能转化为化学能
C. 燃料燃烧时只是将化学能转化为热能
D.由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如图:根据要求填空:
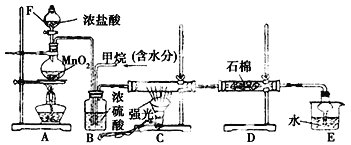
(1)实验室制取Cl2的化学方程式为:____________________。
(2)写出CH4与Cl2生成一氯代物的化学方程式____________________。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③________。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是________________________。
(5)E装置的作用是________。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(6)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法为__________。
(7)该装置还有缺陷,原因是没有进行尾气处理,尾气的主要成分是(双选,填编号)________。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R 是五种短周期元素,原子序数依次增大。X、Y 两元素最高正价与最低负价之和均为 0;Q 与 X 同主族;Z、R 分别是地壳中含量最高的非金属元素和 金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)____________。
(2)X 与 Z 能形成多种化合物,请写出其中既含极性键又含非极性键的物质的分子式_______________。
(3)由以上某些元素组成的化合物 A、B、C、D 有如下转化关系:A![]() B其中,A、B、D 均由三种元素组成,B 为两性不溶物,C 是一种能造成温室效应的气体。D的电子式_____;由 A 与足量 C 反应转化为 B 的离子方程为_________;(4)Q的氢化物与Z的普通氢化物之间的化学反应方程式为:_________;
B其中,A、B、D 均由三种元素组成,B 为两性不溶物,C 是一种能造成温室效应的气体。D的电子式_____;由 A 与足量 C 反应转化为 B 的离子方程为_________;(4)Q的氢化物与Z的普通氢化物之间的化学反应方程式为:_________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com